cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;

地址:北京市丰台区西四环南路35号中都科技大厦10层
《互联网药品信息服务资格证书》 编号:(京)一非经营性一2021一0014
备案序号:京ICP备12047146号和京ICP备16030590号 信息产业部备案管理系统网址

扫
一
扫
© 2026北京远博康惠医药信息咨询有限公司 版权所有
北京远博医药CRO
感谢您关注远博医药微信公众号


© 2026北京远博恒康医药科技有限公司 版权所有
本原则旨在为治疗脂代谢紊乱的药物临床提供指导,在中应同时参考其他相关的指导原则。
脂代谢紊乱指试验室检查的血脂水平异常,并据此进行分类,但这种分类并不能确切反映不同的基因和代谢缺陷,或相关临床疾病。血脂水平可能受其他临床情况的影响,如糖尿病、甲状腺疾病或肾病综合征,在这些情况下首先应治疗基础疾病,一旦这些疾病得到控制,应对血脂水平进行重新评估。
一、引言
脂代谢紊乱最常见的是高胆固醇血症。流行病学证据显示血清胆固醇水平特别是血清LDL胆固醇和冠心病(CHD)风险之间存在强相关性和因果关系,动脉粥样硬化的其他临床表现也与血浆LDL胆固醇水平相关;另外,临床试验也显示降低LDL的治疗可降低发生CHD的风险。“血胆固醇正常”和“高胆固醇血症”之间分界线的确定是人为的。流行病学资料显示,胆固醇水平从非常低到“正常”及高水平的较大范围内都与冠心病的风险连续(可能非线性)相关。
治疗决策不仅基于胆固醇水平,还基于多种危险因素对心血管总体风险的影响。影响LDL胆固醇控制目标的因素主要包括:(1)存在CHD和其他临床形式的动脉粥样硬化;(2)糖尿病;(3)心血管危险因素的数量。
高胆固醇血症可独立存在,也可同时伴随其他的脂代谢紊乱,特别是高甘油三酯血症(“混合性高脂血症”)和低HDL胆固醇等。但脂代谢紊乱也包含单纯的高甘油三酯血症和/或低HDL胆固醇。甘油三酯升高是独立的CHD危险因素,但高甘油三酯的治疗策略视其升高原因及其严重程度而定。低HDL胆固醇水平,不管是否与高甘油三酯结合,也是CHD的一个强的独立危险因素,尽管其治疗目标还有待进一步阐明,但应引起临床医生的注意。虽然目前强调高胆固醇血症,但是对其他脂代谢紊乱也应予以注意。
二、有效性评价标准
(一)血脂水平
虽然理想的调脂药物应显示在预防心血管发病率和死亡率中的有益效应,但这需要大样本长时间的临床试验,因此在原发性高胆固醇血症患者中LDL胆固醇的相对下降可作为有效的替代终点,但不应依此作出关于心血管发病率和死亡率的结论。甘油三酯水平的下降和/或HDL胆固醇的升高也可作为特定目标人群主要终点的一个相应组成部分,但是对这些参数的单独效应原则上不能作为证明新调脂药物有效性的唯一证据,而应与对非HDL胆固醇的效应以及潜在机制联系起来。一种新的调脂药物仅在对心血管和非心血管的死亡率和发病率没有不利影响时才能注册。
(二)血管损伤
尽管心、脑、肾、血管等靶器官的损伤[如中膜厚度(IMT)和斑块稳定性的改变]可能与心血管发病率和死亡率相关,但是调脂药物对靶器官损伤的影响,与病人发病率和死亡率的相关性仍需明确。目前,一种药物(或药物联合使用)对于某一部位的动脉粥样硬化负荷的效应尚不能认为是心血管发病率和死亡率的有效替代终点。这些终点可能提供药物作用机制和临床保护效果的信息,随着这方面的科学越来越多,在特定亚组中这些可能替代使用发病率和死亡率临床终点的临床试验。
(三)发病率和死亡率
治疗脂代谢紊乱的主要目的在于预防与血脂水平相关的心血管疾病的发病率和死亡率(但是在甘油三酯水平非常高的罕见情况下,首要目的是预防急性胰腺炎)。临床试验显示不论其基线胆固醇水平高低,大多数HMG-CoA还原酶抑制剂减少心血管事件(包括卒中)和高心血管危险患者的总死亡率。一些数据也提示,贝特类药物在混合性高脂血症患者及仅有低HDL胆固醇而无高胆固醇血症的冠心病患者中,也有降低冠脉事件发生率的作用。只有在脂代谢紊乱和/或高心血管危险的患者中进行大规模长期临床试验,才能获得死亡率和发病率的阳性结果。如果没有该种临床试验数据,在说明书中应特别提出其在死亡率和发病率方面的获益是未知的。
三、有效性评价的方法
(一)血脂水平
调脂药物的调脂效应应当按治疗前/后血脂水平改变进行评估。所有检查应当在标准的膳食导入期(伴或不伴适当洗脱期)后空腹条件下进行。
在原发性高胆固醇患者中以LDL胆固醇降低作为主要终点,可以支持高胆固醇血症或混合性高脂血症的适应症。其他对胆固醇的药物效益评价指标可以作为次要终点,这些指标的定义应符合公认的标准。
因为甘油三酯、总胆固醇和HDL胆固醇越来越多用于辅助治疗推荐中,这些参数的改变也可以作为次要终点进行。对于某些特殊人群(如糖尿病等)除了LDL胆固醇外,脂代谢紊乱的检查如甘油三酯和HDL胆固醇的改变也可能成为主要疗效指标,其前提是不能对其他脂代谢参数或临床事件有不利影响。其他脂代谢紊乱检查,例如载脂蛋白A1和AII、载脂蛋白B或者apoB和apoA-1比例、脂蛋白(a)仅在认为与临床结局相关时才考虑作为次要有效性检查。对于糖尿病受试者,应当记录治疗前/后血糖控制的改变,因为这可能会影响血脂水平。另外还应认识到除现有定量血脂异常外,其他定性血脂异常(如小而密或氧化LDL)也可能成为新型调脂药物的主要目标。
(二)血管损伤
动脉粥样硬化进展和斑块稳定性能够通过有效和可靠的技术进行检测,例如定量B超、MRI和血管内超声(IVUS)。不管使用哪种技术,其检测方法的标准化和检测结果的准确性应当经过充分的验证,指定部位动脉粥样硬化负荷测量的有效性和可靠性应该准确说明并以文件形式记录保存。目前不能认为这些参数是硬性临床终点的替代品,但是它们可以组成适当的次要终点以支持关于动脉粥样硬化进展或消退的信息。
(三)发病率和死亡率
设计一个以死亡率为临床终点的时,应当把重点放在所有原因死亡率和/或心血管死亡率,并由一个设盲的、独立委员会判定。如果选择心血管死亡率作为(联合)主要终点,那么对非心血管死亡率的效应也应加以考虑。评估心血管死亡率应当考虑器官损伤的症状和体征(如心肌梗死、休克)以及其他治疗措施(如CABG和PTCA的次数和/或其他血管区的介入)。因为已有药物(主要是他汀类药物)的有效性和安全性,安慰剂对照不再适用于大规模和高风险患者的临床试验。
四、患者选择
对于评估新药治疗脂代谢紊乱的有效性,其人群一般取决于药物预期治疗的脂代谢紊乱类型。评估新调脂药物的有效性或安全性主要在患有原发性高胆固醇血症和混合性高脂血症且胆固醇水平中度到重度升高的患者中进行。应当注意性别、人种和年龄的影响。若药物要求用于儿童和18岁以下的青少年时需要进行单独,否则不推荐用于该年龄组。应该包含一定数量的大于65岁的受试者。
对于以临床结果评价为目标的试验,应根据心血管的总体风险选择受试人群,而不论是否存在冠状动脉疾病以及其基线胆固醇水平。应当有足够数量动脉粥样硬化和/或2型糖尿病的临床表现和/或其他表现的患者以便分组统计分析。这些可能包含胆固醇水平处于分界线甚至正常的患者。
当申请特殊适应症时,家族性高胆固醇血症的患者(杂合子突变和纯合子突变)一般应当根据临床、遗传和/或功能性的标准在单独的临床试验中进行。这也适用于其他脂代谢紊乱类型,包括家族型血β脂蛋白异常和高乳糜微粒血症。
五、设计策略
与其他用于心血管疾病药物的临床相比,用于脂代谢紊乱患者的新药原则上没有区别。
在筛选期后,随机分组前必须有一个膳食导入期。试验的入选标准和入选方法的可靠性应当经过验证,应该考虑到目标人群和检测准确性等因素。在单药治疗时,原有的调脂治疗应在该阶段开始时撤药,并需要充分的洗脱。应记录膳食供给、食品及运动习惯,并在整个试验期间维持不变。
(一)药效学
应当至少包含耐受性、作用时间和相关血液动力学参数的评估。进一步的需要根据药物作用机制和动物毒理学数据进行设计,如白内障的临床前期证据和肌病症状体征的发生。
(二)药代动力学
应当与药代动力学相关指导原则的要求相一致。调脂药物的应当特别注意与其他药物药代动力学的相互作用。
(三)治疗性
1.探索性
剂量探索一般应该遵循随机化、安慰剂对照、双盲的原则,且至少3种剂量以便建立临床有效的剂量范围及最佳剂量。对于大多数剂量探索,一般采用固定剂量的平行组设计方法。剂量组的设置应该能显示不同剂量之间调脂效应的差别。在老年人和高风险患者中,剂量调整方案应该清晰阐明。周期一般从4周到3个月。
2.确证性
2.1 单药治疗
在确证性试验中大多数采用活性对照,因为安慰剂对照不再适用于该领域的大型。应当根据药理学分类、调脂效应类型和适应症选择合适的对照,对照药的疗效和安全性应该经过自身的临床试验进行确认,并具备同种适应症。在同一种类药物内进行比较时,应注意对照药的剂量是否合适。非劣性试验界值的设定和临床差异性均应综合考虑。包含安慰剂的三臂(短期)可能是有价值的,这取决于起始治疗中疗效的大小。
确证性试验中,剂量的调整方案须根据在目标人群中进行的剂量探索试验来确定。周期取决于其预期结果,剂量滴定和达到最大效果的时间,但应该至少持续3至12个月。应根据试验方案所确定的用药原则调整剂量,并且每个剂量水平的治疗持续时间应当足够长,以便在进一步改变剂量前评估应答效应。
以临床获益为终点的试验,应该选择已显示临床获益的调脂药物进行比较。这些通常需要较长时间。
2.2 调脂药联合治疗
调脂药物的联合用药应当在任一成分均无充分有效反应的患者中进行专门,采用安慰剂为对照。反应率应根据要求的调脂效应进行定义并符合当前公认的标准。在新药仅用于与现有药物联合用药的情况下,目标人群预期由上市药物标准剂量单药治疗控制不充分的患者组成。原则上,联合用药策略不能根据其对LDL胆固醇和其他脂代谢参数,特别是单独对TG和HDL-C的作用就被批准作为一线治疗,除非申请者能够证明该策略在发病率和死亡率上的获益。
六、安全性评价
临床试验期间发生的所有不良事件必须完整记录,并分别分析不良事件/反应、脱落、治疗期间死亡的患者以及临床试验室结果。
基于药物作用机制以及其他药物中所见的潜在安全性信号,特定靶器官安全性监测应当反映非临床和临床结果。特别注意以下方面:
(一)肝脏
应注意药物性肝炎的症状和体征,并常规检测ALT、胆红素和其他肝脏生化指标,并分别根据平均改变及数值大于1倍和大于3倍正常参考值上限的患者数量进行分析。除非是禁忌症,应当提交既往有肝损伤,特别是肝硬化患者的信息。
(二)肌肉
不同种类的调脂药物均被发现与CK升高及肌肉相应症状。应当特别注意肌病的症状和体征。常规检测CK水平,并分别根据平均改变及数值>l倍、>3倍、>5倍和>l0倍正常参考值上限的患者数量进行分析。由于严重肌病罕见,因此,应考虑上市后监测CK和肌肉症状。
(三)肾脏
临床前数据已提示调脂药物对肾小管细胞存在肾毒性效应,因此临床试验中必须监测肾功能和蛋白尿。
(四)死亡率和心血管发病率的长期效应
在短期、小样本的中,非心血管发病率和死亡率在间可能并不一样(即使是显示阴性效应时),因此要观察对死亡率和心血管发病率的长期效应。不同性别和年龄组足够多的患者群应持续暴露于药物至少一年,但最好更长时间。患者人群应当代表了经常给予调脂药物的临床疾病,例如糖尿病、缺血性心脏病和高血压。应当有充分的安全性数据以排除新药对死亡率的任何可疑不利影响。当药物属于新的作用机制时,这个要求可以获得特异相关性的结果。来自临床项目的关于死亡率和心血管发病率的有效数据应当进行彻底分析,也应考虑临床前数据及来自其他相同类别或不同类别调脂药物的结果。一种新的调脂药物仅在对死亡率和发病率没有不利影响时才能注册。否则,将强制要求进行额外的来阐明药物对这些参数的影响。
七、药物相互作用
应当通过一般的联合药物治疗临床以及特定的临床进行相互作用,药物各成分和活性代谢产物也应加以考虑。不同调脂药物的联合用药可能增强有效性,但也可能增加不良反应,特别是由于药代动力学和/或药效学的相互作用导致发生肌病和/或肝功能障碍。这同样适用于调脂药物与已知导致肝、肌肉和肾脏等器官损伤的非调脂药物联合用药的情况,特别是在具有高心血管事件风险患者中经常合并的药物,例如抗血小板药和口服抗凝血药。特定药物相互作用取决于新药的药代动力学和药效学特性。影响其吸收(如抗酸药)和代谢(如环孢素、细胞色素P450酶抑制剂),以及与维生素K和口服避孕药/激素替代治疗(HRT)的药物相互作用也应加以考虑

治疗脂代谢紊乱药物临床指导原则
2021年10月21日发布



商务拓展部(药品&器械)袁经理
电话:010-83659936 18618362640
邮箱:ybkj045@126.com
人力资源部主任
电话:13146546661
邮箱:ybkj010@126.com
商务总监(药品&器械)薛总
电话:13810708945
邮箱:ybkj027@126.com


◆丰富的临床试验服务经验:
◆熟悉政策法规及审评动态:
◆良好的专家关系:
◆大量临床医院的资源:
◆专业的数据管理:
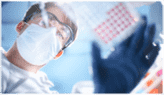
CRO:Contract Research Organization, 出现于上世纪80年代,一种学术性或商业性的科学机构。申办者可委托其执行临床试验中的某些工作和任务,此种委托必须作出书面规定,其目的是通过合同形式向制药企业提供新药临床服务的专业公司。CRO 可以作为制药企业的一种可借用的外部资源,可在短时间内迅速组织起一个具有高度专业化的和具有丰富临床经验的临床队伍,并能降低整个制药企业的管理费用。
 了解更多
了解更多
了解更多
了解更多








我公司承接国内外厂家或公司的委托,从事药物、医疗器械临床代理服务,以下是我公司服务过的部分项目的名称。














北京远博医药CRO成立于2005年,为医疗企业提供临床试验、项目申报、项目管理和信息咨询等的专业化外包服务(CRO服务),主要为专业化服务内容包括:新药(化药、中药和生物制品)的Ⅰ~Ⅳ临床试验、药代动力学(PK)、生物等效性(BE)、医疗器械的临床试验、上市后再评价、中药保护临床试验、药物经济学等项目的监查及项目管理。
专业化人才优势
绝大多数员工拥有专科以上学历
高标准质量管理体系
必须通过国家药监局高级研修学院的GCP培训并获得证书
完善的培训系统
注重对员工的技术培训,积极参加国家药监总局、药审中心、器械审评中心及各学术团体举办的专业培训及会议;
◆丰富的临床试验服务经验:
◆熟悉政策法规及审评动态:
◆良好的专家关系:
◆大量临床医院的资源:
◆专业的数据管理:
◆优秀而稳定的团队:
◆完善的标准操作流程:
◆独立的质量保障部门:
◆灵活多样的服务方式:

































































































































































































































 预约上门洽谈
免费项目咨询
预约上门洽谈
免费项目咨询CRO

北京远博医药

临床试验、一致性评价、BE研究和技术服务的专家
专业为医药企业提供一体化的专业技术服务



临床试验优先选择的CRO
18618362640
010-83659936
全国客服热线