cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;
附件3
C反应蛋白测定试剂盒注册技术审查指导原则
(2016年修订版)
本指导原则旨在指导注册申请人对C反应蛋白测定试剂盒,包括常规C反应蛋白定量检测试剂盒/超敏(高敏)C反应蛋白定量检测试剂盒/全量程C反应蛋白定量检测试剂盒注册申报资料的准备及撰写,同时也为技术审评部门审评注册申报资料提供参考。
本指导原则是对C反应蛋白测定试剂盒的一般要求,申请人应依据产品的具体特性确定其中内容是否适用,若不适用,需具体阐述理由及相应的科学依据,并依据产品的具体特性对注册申报资料的内容进行充实和细化。
本指导原则是供申请人和审查人员使用的指导文件,不涉及注册审批等行政事项,亦不作为法规强制执行,如有能够满足法规要求的其他方法,也可以采用,但应提供详细的研究资料和验证资料。应在遵循相关法规的前提下使用本指导原则。
本指导原则是在现行法规、标准体系及当前认知水平下制定的,随着法规、标准体系的不断完善和科学技术的不断发展,本指导原则相关内容也将适时进行调整。
一、适用范围
本指导原则适用于基于分光光度法原理,利用手工和半自动、全自动生化分析仪,在医学实验室进行对人血清或血浆中的C-反应蛋白进行定量检测所使用的临床化学体外诊断试剂(盒)。
本指导原则不适用于:
1.对C反应蛋白校准品和质控品的评价。
2.各类胶体金标记试纸。
二、注册申报资料要求
(一)综述资料
C-反应蛋白(C-reactive protein,CRP)由肝细胞合成,在胎儿期产生,非母体胎盘传递。其产生机理是:当机体受感染或组织受损伤时巨噬细胞和其他白细胞等被激活,产生白细胞介素-6(IL-6)、白细胞介素-1(IL-1)、肿瘤坏死因子TNF-a等细胞因子及其他介导物,这些细胞因子和介导物到达肝脏,刺激肝细胞和上皮细胞合成CRP。在结构上,CRP含5个多肽链亚单位,非共价地结合为盘形多聚体,分子量为11.5万—14万,CRP是一种典型的急性时相蛋白。全程C反应蛋白包括常规C反应蛋白(常规CRP)和超敏C反应蛋白(超敏CRP)。一次性检测常规CRP和超敏CRP,这种方法被称为全程C反应蛋白检测。常规CRP和超敏CRP在化学本质上无区别,是同一种物质,只是检测方法的定量下限不同。
常规CRP测定包括定性、半定量和定量分析,可用于评价感染,组织损伤和炎症性疾病。对于常规的CRP测定,参考值通常被认为是临床上含量高于10毫克/升。在健康人群血液中CRP水平低于5毫克/升,而在各种条件下,急性炎症4—8小时内,CRP值达到约20至500毫克/升。常规CRP作为急性炎症评估指标比红细胞沉降率(ESR)和白细胞计数更敏感、更可靠。
超敏C反应蛋白线性范围低端低于常规CRP,这种较低的范围可扩大使用适应症,C反应蛋白是非特异性的,必须结合临床症状综合评估,不能作为特定的疾病或疾病的风险的确诊依据。
图1 超敏CRP与常规CRP的区别
超敏C反应蛋白常见的用途可作为心血管疾病风险识别的辅助手段。配合传统的急性冠脉综合征临床诊断使用,可作为冠状动脉疾病或急性冠脉综合征复发的预警指示物。
图2 超敏CRP的临床意义
表1 各种CRP的区别及性能要求
常规CRP
超敏CRP
用途
感染,组织损伤和炎症性疾病的评价。提供炎症性疾病的诊断,治疗和监控的信息
是区分低水平炎症状态的灵敏指标, 血清hs-CRP 水平与动脉粥样硬化及急性脑梗死( ACI) 等心脑血管疾病的发生、严重程度及预后密切相关
参考值范 围
参考值范围: 约10mg/ L
健康人群:≤ 5mg / L
急性范围: 20—500 mg/L
参考值范围: 1mg/L
推荐线性范围
≥ 5mg/L到上限
0.5 mg/L 到≤ 10.0mg/L
灵敏度
明确在线性范围低端的性能
确定定量限(功能灵敏度)
综述资料主要包括CRP的代谢、产品预期用途、产品描述、参考品的详细溯源性、有关生物安全性的说明、研究结果的总结评价以及同类产品上市情况介绍等内容,其中同类产品上市情况介绍部分应着重从方法学、临床应用情况、性能指标等方面写明拟申报产品与目前市场上已获批准的同类产品之间的异同。应符合《体外诊断试剂注册管理办法》(国家食品药品监督管理总局令第5号)和《关于公布体外诊断试剂注册申报资料要求和批准证明文件格式的公告》(国家食品药品监督管理总局公告2014年第44号)的相关要求。
人源性材料须对有关传染病(HIV、HBV、HCV、梅毒等)病原体检测予以说明,并提供相关的证明文件。其他动物源及微生物来源的材料,应当提供相应的说明文件,证明其在产品运输、使用过程中对使用者和环境是安全的,并对上述原材料所采用的灭活等试验方法予以说明。
1.试剂盒所用抗体的制备、筛选、纯化以及鉴定等详细试验资料。如抗体为申请人自制,则应详述抗体的名称及生物学来源,申请人对该抗体技术指标的要求(如外观、纯度、蛋白浓度、效价等),确定该抗体作为主要原材料的依据;如抗体为申请人外购,则应详述抗体的名称及生物学来源,外购方名称,提交外购方出具的抗体性能指标及检验证书,详述申请人对该抗体技术指标的要求以及申请人确定该抗体作为主要原材料的依据。
2.其他主要原辅料的选择及验证资料,如包被板、反应缓冲液等,申请人应详述每一原辅料技术指标的要求以及确定该原辅料作为主要原辅料的依据。若为外购,应详述每一原辅料的外购方名称并提交外购方出具的每一原辅料性能指标及检验证书。
3.企业内部参考品的原料选择、制备、定值过程及试验资料。
4.添加上述原材料、辅料的详细信息请以附录的形式呈现。
(三)主要生产工艺及反应体系的研究资料(如需提供)
1.主要生产工艺介绍,可以流程图方式表示,并简要说明主要生产工艺的确定依据。
2.产品反应原理介绍。
3.抗体包被/致敏工艺研究:申请人应考虑如包被液量、浓度、时间、温度等指标对产品性能的影响,通过试验确定上述指标的最佳组合。
4.实验体系反应条件确定:申请人因考虑反应时间、反应温度、pH值等条件对产品性能的影响,通过试验确定上述条件的最佳组合。
5.体系中样品加样方式及加样量确定:申请人应考虑样品加样方式、加样量对产品检测结果的影响,通过实验确定最佳的加样方式及加样量。如样本需采取稀释或其他必要的方法进行处理后方可用于最终检测,申请人还应对可用于样本稀释的物质或处理方法进行研究,通过试验确定最终选择的用于样本稀释的物质或处理方法。确定反应所需其他物质用量(标准品、酶标物、底物等)的研究资料。固相载体、显色(发光)系统、酶作用底物等的介绍。
6.不同适用机型的反应条件如果有差异应分别详述。
(四)分析性能评估资料
企业应提交原厂在产品研制阶段对试剂盒进行的所有性能验证的研究资料,包括具体研究方法、实验数据、质控标准、统计分析等详细资料。对于C反应蛋白定量检测试剂盒建议多批产品对以下分析性能进行研究:分析灵敏度、准确度、特异性、线性范围、精密度(批间、批内)等指标,具体研究方法建议参考相关指导原则。
对于适用多个机型的产品,应提供如产品说明书【适用机型】项中所列的所有型号仪器的性能评估资料。
1.试剂空白吸光度
适用时,用纯化水作为样本重复测定2次,计算试剂空白吸光度(A),测定结果均值应符合产品技术要求性能指标的要求。
2.分析灵敏度
测定一份浓度接近40 mg/L的样品,重复测定2次,计算该样本产生的吸光度改变与空白吸光度改变的差值(△A),取2次结果的均值,等比换算出浓度为40mg/L的CRP所产生的吸光度差值(△A),结果应符合产品技术要求性能指标的要求。
测定一份浓度接近5 mg/L的样品,重复测定2次,计算该样本产生的吸光度改变与空白吸光度改变的差值(△A),取2次结果的均值,等比换算出浓度为5mg/L的CRP所产生的吸光度差值(△A),结果应符合产品技术要求性能指标的要求。
3.检出限
生产企业应提供CRP试剂盒的空白限、检出限及参考区间等相关信息。根据生产企业提供信息,对5份浓度近似最低检出限(LOD)的低值样本进行检测,每份样本检测5次,对检测结果按照大小进行排序,符合如下条件,即可认为生产企业提供的空白限和检出限的设置基本合理,结果符合产品技术要求性能指标的要求。
(1)低于生产企业提供的空白限数值的检测结果的数量应小于等于3个;
(2)适用时,无高于生产企业提供的参考区间下限的检测结果。
4.准确度
(1)总则
可采用相对偏差、企业参考品测试和比对试验之一测试试剂(盒)的准确度,应符合产品技术要求性能指标的要求; 如适用,优先采用相对偏差的方法。
(2)相对偏差
根据生产企业提供的试剂盒线性区间,将能用于评价常规方法的参考物质作为样本,合理设置2—3个浓度,将其作为样本按照待测试剂盒说明书的步骤进行检测,每个样品重复测定3次,测试结果记为(Xi),按公式(1)分别计算相对偏差(Bi),如果3次结果都符合产品技术要求性能指标的要求,即判为合格。如果大于等于2次的结果不符合,即判为不合格。如果有1次结果不符合要求,则应重新连续测试20次,并分别按照公式(1)计算相对偏差,如果大于等于19次测试的结果符合产品技术要求性能指标的要求,即判为合格,准确度符合产品技术要求性能指标的要求。
Bi=(Xi-T)/T×100% (1)
式中:
Bi—相对偏差;
Xi—测量浓度;
T—标定浓度。
(3)企业参考品测试
由生产企业提供企业参考品,按照常规样本进行检测,每份样本测定3次,测试结果记为(Xi),按公式(1)分别计算相对偏差(Bi),结果应符合产品技术要求性能指标的要求。
5.线性
将接近线性区间上限的高值样本按一定比例稀释为至少5个浓度,其中低值浓度的样本须接近线性区间的下限。对每一浓度的样本至少重复测定2次,计算其平均值,将测定浓度的平均值与理论浓度或稀释比例用最小二乘法进行直线拟合,得到线性回归方程,并计算线性相关系数r及绝对偏差或相对偏差,结果应符合产品技术要求性能指标的要求。
6.重复性
用同一批号试剂盒,对2—3个不同浓度的样品分别重复测定10次,计算10次测定结果的平均值(M)和标准差(SD),根据公式(2)得出变异系数(CV),结果应符合产品技术要求性能指标的要求。
CV=SD/M×100% (2)
式中:
CV—变异系数;
SD—10次测量结果的标准差;
M—10次测量结果的平均值。
7.批间差
用三个不同批号试剂盒,对2—3个不同浓度的样品分别重复测定10次,计算每个浓度样本每批号10次测量结果的平均值(Xi,i=1、2、3)及每个浓度样本三个批号30次测量结果的总平均值(XT),根据公式(3)得出批间相对极差(R),结果应符合产品技术要求性能指标的要求。
R=(Xmax-Xmin)/XT×100% (3)
式中:
R—批间相对极差;
Xmax—Xi的最大值,i=1、2、3;
Xmin—Xi的最小值,i=1、2、3;
XT—每个浓度样本30次测量结果的平均值。
8.分析特异性
(1)交叉反应:易产生交叉反应的其他抗原、抗体及嗜异性抗体等的验证情况;
(2)干扰物质:样本中常见干扰物质对检测结果的影响,如高脂、黄疸、类风湿因子、抗凝剂等干扰因子的研究(结果应量化表示,禁用轻度、严重的模糊表述);
(3)药物影响:常见相关治疗药物对检测结果的影响。
9.钩状(Hook)效应(如有):说明不会产生Hook效应的浓度上限或相关研究,如需稀释,应注明对稀释液的要求、最佳或最大稀释比例。
10.质控品性能要求(如有)
(1)定值质控品测量准确度
应至少给出一种用校准品校准测量程序后测定该定值质控品的试验方法。
(2)均一性
通常取同批号的一定数量最小包装单元的校准品、质控品,每包装单元测试1次,按下面的公式计算测试结果的平均值()和标准差S1;另用上述校准品、质控品中的1个最小包装单元连续测试相同次数,计算测试结果的平均值()和标准差S2;按下列各公式计算瓶间重复性CV%,所有参数的瓶间重复性结果均应符合要求。最小装量不够完成瓶间差检测的可只进行批内精密度检测。
公式 1
公式 2
公式 3
公式 4
当S1<S2时,令CV瓶间=0
式中:
----平均值;
S----标准差;
n----测量次数;
xi----指定参数第i 次测量值。
11.生物安全性(如适用)
校准品、质控品如含人源性成分,用经过国家批检合格的以下四种体外诊断试剂盒对该试剂盒的校准品、质控分别进行检测:a)人类免疫缺陷病毒抗体诊断试剂盒;b)丙型肝炎病毒抗体诊断试剂盒;c)乙型肝炎病毒表面抗原诊断试剂盒,HIV抗体、HCV抗体和HBsAg应为阴性;d)梅毒螺旋抗体诊断试剂盒,HIV抗体、HCV抗体、HBsAg和TP抗体应为阴性。
(五)参考区间确定资料
阳性判断值或参考区间确定所采用的样本来源、确定方法及详细的试验资料。建议参考CLSI/NCCLS C28-A2。
稳定性研究资料主要涉及两部分内容,申报试剂的稳定性和适用样本的稳定性研究。前者主要包括实时稳定性(有效期)、运输稳定性、开瓶稳定性及冻融次数限制等研究,申请人可根据实际需要选择合理的稳定性研究方案。稳定性研究资料应包括研究方法的确定依据、具体的实施方案、详细的研究数据以及结论。对于实时、运输及开瓶稳定性研究,应提供至少三批样品在实际储存条件下保存至成品有效期后的研究资料。
试剂稳定性和样本稳定性两部分内容的研究结果均应在说明书【储存条件及有效期】和【样本要求】两项中进行详细说明。
(七)生产及自检记录
提供连续三批产品生产及自检记录的复印件。
(八)临床评价资料
1.研究方法
选择境内已批准上市、临床普遍认为质量较好的同类产品作为参比试剂,采用拟申报产品(以下称考核试剂)与之进行对比试验研究,证明本品与已上市产品等效或优于已上市产品。建议企业尽量选择方法学相同、线性范围及精密度等性能接近的同类试剂作为参比试剂。同时应充分了解所选择产品的技术信息,包括方法学、临床预期用途、主要性能指标、校准品的溯源情况、推荐的阳性判断值或参考区间等,以便对试验结果进行科学的分析。且临床试验必须符合赫尔辛基宣言的伦理学准则,必须获得临床试验机构伦理委员会的同意。
2.临床研究单位的选择
申请人应当选定不少于2家(含2家)获得国家食品药品监督管理总局资质认可的临床试验机构,按照有关规定开展临床试验。
申请人应根据产品特点及其预期用途,综合不同地区人种、流行病学背景、病原微生物的特性等因素选择临床试验机构。临床试验机构必须具有与试验用体外诊断试剂相适应的专业技术人员及仪器设备,并能够确保该项试验的实施。
申请人应当在临床试验前制定文件明确各方的职责分工,与各临床试验机构协商制定统一的临床试验方案,按照临床试验方案组织制定标准操作规程,并组织对参加试验的所有研究者进行临床试验方案和试验用体外诊断试剂使用的培训,以确保临床试验方案和试验用体外诊断试剂操作的一致性,并在临床试验过程中促进各研究者之间的沟通。
在临床试验开始前,申请人应与临床试验工作人员进行临床试验的预试验,使其熟悉并掌握该产品所适用的仪器、操作方法、技术性能等,以最大限度地控制试验误差。
在临床试验过程中,申请人应考虑吸收流行病学、统计学、临床医学、检验医学等方面专业人员(或知识),以保证临床试验科学、合理地开展。
临床研究单位应有能力提供临床评价所需的各类样本,实验操作人员有足够的时间熟悉检测系统的各环节(仪器、试剂、质控及操作程序等),熟悉评价方案。在整个实验中,考核试剂和参比试剂都应处于有效的质量控制下,定期对仪器进行校准,最大限度保证试验数据的准确性及可重复性。
不同的临床单位应使用同一批考核试剂进行临床试验,以便对数据进行科学客观的统计分析。
3.临床试验方案
临床试验实施前,研究人员应从流行病学、统计学、临床医学、检验医学等多方面考虑,设计科学合理的临床研究方案。各临床研究机构的方案设置应基本一致,且保证在整个临床试验过程中遵循预定的方案实施,不可随意改动。整个试验过程应在临床研究机构的实验室内并由本实验室的技术人员操作完成,申报单位的技术人员除进行必要的技术指导外,不得随意干涉实验进程,尤其是数据收集过程。
试验方案中应确定严格的病例纳入/排除标准,任何已经入选的病例再被排除出临床研究都应记录在案并明确说明原因。在试验操作过程中和判定试验结果时应采用盲法及样本随机分配以保证试验结果的客观性。对于新试剂的动态监测研究,应在方案中明确前后两次浓度变化有临床意义的标准。临床试验中所涉及的样本类型应与产品说明书一致,且每种样本类型例数的选择应符合基本的统计学要求。各研究单位选用的参比试剂及所用机型应一致,以便进行合理的统计学分析。
开展体外诊断试剂临床试验,申请人应当按照试验用体外诊断试剂的类别、风险、预期用途等特性,组织制定科学、合理的临床试验方案。一般应当包括以下内容:
(1)一般信息(包括产品信息、临床试验开展的时间和人员等相关信息、申请人相关信息等);
(2)临床试验的背景资料;
(3)试验目的;
(4)试验设计;
(5)评价方法;
(6)统计方法;
(7)对临床试验方案修正的规定;
(8)临床试验涉及的伦理问题和说明、《知情同意书》文本(如有);
(9)数据处理与记录保存;
(10)其他需要说明的内容。
4.研究对象的选择
(1)临床试验样本量的确定:申请人或临床研究者应根据产品临床使用目的,与该改产品相关疾病的临床发生率确定临床研究的样本量。在符合指导原则有关最低样本要求的前提下,还应符合统计学要求。
①临床研究的总样本数至少为200例。
②应考虑样本量的分布。样本量的选择应符合统计学及相关指导原则的要求。
③样本浓度应覆盖考核试剂检测范围,尽可能均匀分布。尽可能使40%样本的测定值处于参考区间以外,但在测量范围内。
(2)变更事项相关的临床试验:涉及产品检测条件优化、增加与原样本类型具有可比性的其他样本类型等变更事项,产品临床试验总样本数至少为100例,并在至少2家(含2家)临床试验机构开展临床试验;变更抗原、抗体等主要原材料的供应商、阳性判断值或参考区间的变化及增加临床适应症等变更事项,应根据产品具体变更情况,酌情增加临床试验总样本数。
(3)建议在临床试验中选择部分含干扰物质的标本进行对比研究,包括高脂、溶血、黄疸的样本、类风湿因子阳性样本,易共存的其他急性炎症时相因子同时升高的患者标本,以从临床角度验证试剂的特异性。
5.统计学分析
对临床试验结果的统计应选择合适的统计方法,如相关分析、线性回归、受试者工作特征(ROC)曲线分析等。对于对比实验的等效性研究,最常用是对考核试剂和参比试剂两组检测结果的相关及线性回归分析,应重点观察相关系数(r值)或判定系数(R2)、回归拟合方程(斜率和y轴截距)等指标。结合临床试验数据的正/偏态分布情况,建议统计学负责人选择合理的统计学方法进行分析,统计分析应可以证明两种方法的检测结果无明显统计学差异。在临床研究方案中应明确统计检验假设,即评价考核试剂与参比试剂是否等效的标准。
6.结果差异样本的验证
对于比较研究试验中测定结果不符的样本,应采用“金标准”或其他合理的方法进行复核,以便对临床试验结果进行分析。如无需复核,应详细说明理由。
7.临床试验总结报告撰写
根据《关于发布体外诊断试剂临床试验技术指导原则的通告》(国家食品药品监督管理总局通告2014年第16号)的要求,临床试验报告应该对试验的整体设计及各个关键点给予清晰、完整的阐述,应该对整个临床试验实施过程、结果分析、结论等进行条理分明的描述,并应包括必要的基础数据和统计分析方法。建议在临床总结报告中对以下内容进行详述。
申请人或临床试验牵头单位应对各临床试验机构的报告进行汇总,并完成临床试验总结报告。临床试验报告的格式及内容如下:
7.1首篇
首篇是每份临床试验报告的第一部分,所有临床试验报告均应包含该部分内容。
7.1.1封面标题
包括试验用体外诊断试剂的通用名称、试验开始日期、试验完成日期、主要研究者(签名)、临床试验机构(盖章)、统计学负责人签名及单位盖章、申请人(盖章)、申请人的联系人及联系方式、报告日期、原始资料保存地点。
7.1.2目录
列出整个临床试验报告的内容目录和对应页码。
7.1.3研究摘要
对临床试验情况进行简单的介绍。
7.1.4试验研究人员
列出临床试验主要研究人员的姓名、单位、在研究中的职责及其简历(列于附件中),主要研究人员包括主要研究者及各单位的主要参加人员、统计学负责人、临床试验报告的撰写人。
7.1.5缩略语
临床试验报告中所用的缩略语的全称。
7.2正文内容和报告格式
7.2.1基本内容
7.2.1.1引言。
介绍与临床试验产品有关的背景情况:包括(1)被测物的来源、生物及理化性质;(2)临床预期使用目的,所针对的目标适应症人群,目前针对该适应症所采用的临床或实验室诊断方法等;(3)所采用的方法、原理、技术要求等;(4)国内外已批准上市产品的应用现状等。说明申请人和临床试验机构间的合作关系。
7.2.1.2研究目的。
说明本临床试验所要达到的目的。
7.2.1.3试验管理。
对试验管理结构的描述。
管理结构包括主要研究者、主要参加人员、实验室质量控制情况、统计/数据管理情况以及试验中发生的问题及其处理措施等。
7.2.1.4试验设计。
7.2.1.4.1试验总体设计及方案的描述。
试验的总体设计和方案的描述应清晰、简洁,必要时采用图表等直观的方式。试验进行时方案修改的情况和任何方案以外的信息来源也应详细叙述。应包括:
(1)临床试验的整体管理情况、临床研究单位选择、临床主要研究人员简介等基本情况介绍;
(2)病例纳入/排除标准、不同年龄段人群的预期选择例数及标准;
(3)样本类型,样本的收集、处理及保存等;
(4)统计学方法、统计软件、评价统计结果的标准
7.2.1.4.2试验设计及试验方法选择。
试验设计中应包括以下内容:
(1)样本量及样本量确定的依据。
(2)样本选择依据、入选标准、排除标准和剔除标准。
(3)样本采集、保存、运输方法等。
(4)对比试剂的确立。
(5)临床试验用所有产品的名称、规格、来源、批号、效期及保存条件,对比试剂的注册情况。考核试剂和参比试剂的名称、批号、有效期及所用机型等信息。
(6)质量控制方法。对质量控制方法进行简要的阐述。试验人员培训、仪器日常维护、仪器校准、质控品运行情况,对检测精密度、质控品回收(或测量值)、抽查结果评估;
(7)临床试验数据的统计分析方法。对各研究单位的病例数、病种分布情况进行总合,建议以列表或图示方式给出具体例数及百分比。
①数据预处理、差异数据的重新检测或第三方验证以及是否纳入最终数据统计、对异常值或缺失值的处理、研究过程中是否涉及对方案的修改。
②定量值相关性和一致性分析
用回归分析验证两种试剂结果的相关性,以y=a+bx和R2的形式给出回归分析的拟合方程,其中:y是考核试剂结果,x是参比试剂结果,b是方程斜率,a是y轴截距,R2是判定系数,同时应给出b的95%(或99%)置信区间,定量值结果应无明显统计学差异。
(8)具体试验过程,样本检测、数据收集、样本长期保存、结果不一致样本的校验等。
(9)试验过程中方案的修改。
一般情况下,临床试验方案不宜更改。试验过程中对方案的任何修改均应说明,对更改的时间、理由、更改过程及有无备案进行详细阐述并论证其对整个研究结果评价的影响。
7.2.1.5临床试验结果及分析。
7.2.1.6讨论和结论。对总体结果进行总结性描述并简要分析试验结果,对本次临床研究有无特别说明,最后得出临床试验结论。
7.2.2有关临床试验中特别情况的说明
7.2.3附件
7.2.3.1临床试验中所采用的其他试验方法或其他诊断试剂产品的基本信息,如试验方法、诊断试剂产品来源、产品说明书及注册批准情况。
7.2.3.2临床试验中的所有试验数据,需由临床试验操作者、复核者签字,临床试验机构盖章(封面盖章和骑缝章)。
7.2.3.3主要参考文献。
7.2.3.4主要研究者简历。
7.2.3.5申请人需要说明的其他情况等。
(九)产品风险分析资料
对体外诊断试剂产品寿命周期的各个环节,从预期用途、可能的使用错误、与安全性有关的特征、已知和可预见的危害等方面的判定以及对患者风险的估计进行风险分析、风险评价和相应的风险控制基础上,形成风险管理报告。应当符合相关行业标准的要求。
(十)产品技术要求
拟定产品技术要求应符合《体外诊断试剂注册管理办法》、《体外诊断试剂注册申报资料要求和批准证明文件格式》、《关于发布医疗器械产品技术要求编写指导原则的通告》(国家食品药品监督管理总局通告2014年第9号)的相关规定。作为定量检测试剂盒,C反应蛋白产品的注册检测应主要包括以下性能指标:外观检查、物理检查、准确度、线性范围、分析灵敏度/检出限(空白限)、精密度(批间、重复性)、校准品溯源性、质控品测量准确度及均一性、生物安全性(如适用)等。如果拟申报试剂已有相应的专用国家/行业标准或相应方法学的通用标准要求发布,则企业标准的要求不得低于上述标准要求。
1.产品性能指标详述以下性能指标:
注1:由于C反应蛋白目前尚无国家参考品,故选用国际约定、行业参考品或企业内部参考品,以后国家参考品若建立,采用国家参考品。
注2:对线性范围、分析灵敏度等的最低要求见表1。
1.1外观
应根据产品的包装特点规定适当的外观要求。一般应有试剂盒各组份组成、性状;内、外包装、标签清晰等的要求。
1.1.1试剂盒应组分齐全,内外包装均应完整,标签清晰;
1.1.2液体试剂无渗漏,冻干组分呈疏松体,复溶后液体均匀(无肉眼可见颗粒、无沉淀)。
1.2试剂空白吸光度
适用时,生产企业应规定试剂空白吸光度,并符合相应要求。
1.3分析灵敏度
1.3.1常规C反应蛋白定量检测试剂盒、全量程C反应蛋白定量检测试剂盒,在生产企业规定波长(光径1cm),对应于浓度为40mg/L的CRP所引起的吸光度差值(△A)的绝对值应在0.05—0.50的范围内。
1.3.2超敏(高敏)C反应蛋白定量检测试剂盒,在生产企业规定波长(光径1 cm),对应于浓度为5mg/L的CRP所引起的吸光度差值(△A)的绝对值应在0.05—0.50的范围内。
注:仅适用于免疫透射比浊法
1.4检出限
生产企业应提供CRP试剂(盒)的检出限,常规C反应蛋白定量检测试剂盒检出限不高于5mg/L,超敏(高敏)C反应蛋白定量检测试剂盒、全量程C反应蛋白定量检测试剂盒检出限不高于0.5mg/L。
1.5准确度
准确度应符合如下要求之一:
1.5.1相对偏差:用可用于评价常规方法的有证参考物质(CRM)作为样本进行检测,其测量结果的相对偏差应不超过±15%。
1.5.2企业参考品测试:对具有溯源性的企业参考品进行检测,其测量结果的相对偏差应不超过±10%。
1.6线性
生产企业应规定CRP试剂(盒)的线性区间,
1.6.1线性区间内,线性相关系数|r|应不小于0.990;
1.6.2超敏C反应蛋白定量检测试剂(盒)线性区间不窄于 [0.5,10] mg/L;
1.6.3常规C反应蛋白定量检测试剂(盒)线性区间不窄于 [5,80] mg/L;
1.6.4全量程C反应蛋白定量检测试剂盒线性区间不窄于[0.5,80] mg/L。
1.6.5应规定线性区间内的线性偏差,可根据实际情况,在线性区间的不同分段以相对偏差或绝对偏差表达。
1.7重复性
在线性区间范围内,选择2—3个不同浓度水平的样本,浓度选择可参考医学决定水平,代表正常值和异常值水平。各重复检测10次,其变异系数(CV)应不大于10%。
1.8批间差
用三个批号试剂盒分别选择2—3个不同浓度水平的样本,则三个批号试剂盒之间的批间相对极差应不大于15%。
1.9稳定性
可对效期稳定性和热稳定性进行验证。
1.9.1效期稳定性
生产企业应规定试剂(盒)的有效期。取效期末的试剂盒检测其试剂空白吸光度、分析灵敏度、检出限、准确度、线性和重复性等符合相应指标的要求;
1.9.2热稳定性试验(如适用)
取有效期内的试剂盒在37℃放置一定时间,检测其试剂空白吸光度、分析灵敏度、检出限、准确度、线性和重复性等,应符合相应指标的要求。
注1:热稳定性试验不能用于推导产品有效期,除非是采用基于大量的稳定性研究数据建立的推导公式;
注2:一般地,效期为1年时选择不超过1个月的产品,效期为半年时选择不超过半个月的产品,以此类推。但如超过规定时间,产品符合要求时也可以接受;
注3:根据产品特性可选择上述方法的任意组合,但所选用方法宜能验证产品的稳定性,以保证在效期内产品性能符合要求。
1.10质控品性能要求(如有)
1.10.1定值质控品测量准确度
1.10.2均一性
1.11生物安全性(如适用)
2.检验方法
检验方法的制定应与相应的性能指标相适应。应优先考虑采用公认的或已颁布的标准检验方法。检验方法的制定需保证具有可重现性和可操作性,需要时明确样品的制备方法,必要时可附相应图示进行说明,文本较大的可以附录形式提供。
对于体外诊断试剂类产品,检验方法中还应明确说明采用的参考品/标准品、样本制备方法、使用的试剂批次和数量、试验次数、计算方法。
3.附录
应提供所用CRP校准品的来源、赋值过程的详细溯源性报告以及测量不确定度等内容。
(十一)产品注册检验报告
根据《体外诊断试剂注册管理办法》要求,首次申请注册的第二类产品应该在具有相应医疗器械检验资质和承检范围的医疗器械检测机构进行注册检测。注册检验时优先使用有证参考物质,若无法获取可以使用企业参考品。
(十二)产品说明书
说明书承载了产品预期用途、标本采集及处理、实验方法、检测结果解释以及注意事项等重要信息,是指导实验室工作人员正确操作、临床医生针对检验结果给出合理医学解释的重要依据,因此,产品说明书是体外诊断试剂注册申报最重要的文件之一。产品说明书的格式应符合《关于发布体外诊断试剂说明书编写指导原则的通告》(国家食品药品监督管理总局通告2014年第17号)的要求,境外试剂的中文说明书除格式要求外,其内容应尽量保持与原文说明书的一致性,翻译力求准确且符合中文表达习惯。产品说明书的所有内容均应与申请人提交的注册申报资料中的相关研究结果保持一致,如某些内容引用自参考文献,则应以规范格式对此内容进行标注,并单独列明文献的相关信息。
结合《体外诊断试剂说明书编写指导原则》的要求,下面对C反应蛋白定量检测试剂盒说明书的重点内容进行详细说明,以指导注册申报人员更合理地完成说明书编制。
1.【预期用途】
C反应蛋白定量检测试剂盒用于体外定量检测血清、血浆、全血中的C反应蛋白浓度,适用的样本类型应结合实际的临床研究情况进行确认。
第二段应阐述与该注册产品预期用途相关的临床适应症及详细背景资料。
注:C反应蛋白包括常规C反应蛋白(CRP)、超敏CRP(hsCRP),全程C反应蛋白,具体根据临床试验核定。
2.【主要组成成分】
(1)说明试剂包含主要组分及所用原材料的名称、数量、比例或浓度等信息。
(2)试剂中不包含但对该项检测必须的组分,申请人应列出相关试剂/耗材的名称、货号及其他相关信息。
(3)试剂盒中不包含质控品、校准品或其他耗材,应说明经验证后推荐配合使用的商品化质控品、校准品或其他耗材的制造商、产品名称以及产品货号等详细信息;如包含校准品和/或质控品,应说明其主要组成成分及其生物学来源,校准品应注明其定值及溯源性,质控品应有合适的检测范围。
(4)应注明不同批号试剂盒中各组分可否互换。
3.【储存条件及有效期】
试剂的效期稳定性、开封稳定性、运输稳定性等信息作详细介绍。并对开封后未使用产品允许暴露于空气中的温度、湿度及效期等条件予以明确。
注:保存条件不应有模糊表述,如“室温”,应明确贮存温度,如2℃—8℃,有效期12个月。稳定期限应以月或日或小时为单位。
4.【样本要求】重点明确以下内容:
(1)样本采集:采集时间点是否受临床症状、用药及进食情况等因素的影响,具体采集部位及类型,详述具体的操作方法或列出相关操作指南文件以指导使用者(最好能够给出具体图示),尽量减少由于样本采集或处理不当对实验造成的影响。
(2)样本处理及保存:样本的保存条件及期限(短期、长期)、运输条件等。冷藏/冷冻样本检测前是否须恢复室温,冻融次数限制。
(3)样本的最大可稀释倍数。
(4)样本适用的抗凝剂类型及实验反应温度。
5.【适用机型】所有适用的仪器型号,并提供与仪器有关的重要信息以指导用户操作。
6.【检验方法】详细说明实验操作的各个步骤,包括:
(1)实验条件:实验环境的温度、湿度等注意事项,检验试剂及样本复温、试剂孵育温度及试剂空白等要求。
(2)试剂使用方法(手工/半自动/全自动)、注意事项。
(3)详述待测样品的预处理方法、步骤及注意事项。
(4)明确样本满足临床检测需要的加样量及观察时间。
(5)质量控制程序:质控品的使用、质量控制方法。
(6)校准程序:校准品的准备和使用,校准曲线的绘制方法。
(7)应详述实验结果的计算方法,以及与国际单位的换算公式(如适用)。
7.【参考区间】
应注明常用样本类型的参考区间,简单介绍设定该参考区间所选健康人群的区域特征,建议注明以下字样“由于地理、人种、性别及年龄等差异,建议各实验室建立自己的参考值区间”。并简要说明参考区间的确定方法。
8.【检验结果的解释】
结合质控品对所有可能出现的结果进行合理的解释。本试剂的检测结果仅供临床参考,对患者的临床诊治应结合其症状/体征、病史、其他实验室检查及治疗反应等情况综合考虑。明确有可能存在的数值升高因素及数值降低因素,明确说明对何种条件下需要进行重复检测,以及在重复检测时对待测样本可能采取的优化条件等进行详述。
9.【检验方法局限性】
(1)干扰物质及钩状效应(HOOK效应,如适用)对检测结果的影响。
(2)操作时必须严格按照操作规程,精心操作才能得到正确结果,对操作程序作任何修改都可能影响结果。
(3)有关假阴性结果的可能性分析。
某些未知成分屏蔽了抗原决定簇使之无法与抗体结合;C反应蛋白抗原随着样本放置时间的延长和外界温度上升逐渐降解无法被抗体识别;不合理的样本采集、转运及处理、样本中被测物质浓度过低等均有可能导致假阴性结果。
10.【产品性能指标】
说明该产品的主要性能指标。
11.【注意事项】应至少包括以下内容:
(1)有关人源组分(如有)的警告,如:试剂内质控品或其他可能含有人源物质的组分,虽已经通过了HBs-Ag、HIV1/2-Ab、HCV-Ab、TP-Ab等项目的检测,但截至目前,没有任何一项检测可以确保绝对安全,故仍应将这些组分作为潜在传染源对待。
(2)建议实验室的环境要求,如温度、湿度、电磁环境等。
(3)对采集样本的要求,建议使用新鲜血液,不建议使用高脂乳糜样、黄疸、高类风湿因子样本,勿使用溶血样本,明确样本的处理办法。明确特异性抗体有无干扰。
(4)对所有样本和反应废弃物都视为传染源进行处理。
三、名词解释
(一)分析特异性(Analytical Specificity):测量程序只测量被测量物的能力。分析特异性用于描述检测程序在样本中有其他物质存在时只测量被测量物的能力。通常以一个被评估的潜在干扰物清单来描述,并给出在特定医学相关浓度值水平的分析干扰程度。
(二)精密度(Precision):在规定条件下,相互独立的测试结果之间的一致程度。精密度的程度是用统计学方法得到的测量不精密度的数字形式表示,如标准差(SD)和变异系数(CV)。
四、参考文献
(六)How to Define and Determine Reference Intervals in the Clinical Laboratory”; Approved Guideline, Second Edition 2000,CLSI/NCCLS C28-A2
C反应蛋白测定试剂盒注册
技术审查指导原则(2016修订版)编制说明
一、指导原则编写目的
(一)本指导原则编写的目的是用于指导和规范C反应蛋白测定试剂盒产品注册申报过程中审查人员对注册材料的技术审评;同时也可指导注册申请人的产品注册申报。
(二)本指导原则旨在让初次接触该类产品的注册审查人员对产品机理、结构、主要性能、预期用途等各个方面有所了解,同时让技术审查人员在产品注册技术审评时把握基本的尺度,对产品安全性、有效性作出系统评价。
二、指导原则编写依据
(一)《医疗器械监督管理条例》(国务院令第650号)
(二)《体外诊断试剂注册管理办法》(国家食品药品监督管理总局令第5号)
(三)《关于发布体外诊断试剂临床试验技术指导原则的通告》(国家食品药品监督管理总局通告2014年第16号)
(四)《关于发布体外诊断试剂说明书编写指导原则的通告》(国家食品药品监督管理总局通告2014年第17号)
(五)《中国生物制品规程》
(六)国家食品药品监督管理部门发布的其他规范性文件
(七)现行的国家标准和行业标准
三、指导原则部分内容编写考虑
(一)产品的主要技术指标制定主要参考相关国家标准、行业标准GB/T 26124-2011临床化学体外诊断试剂(盒)、YY/T 1183-2010《酶联免疫吸附法试剂(盒)》。
(二)为了提高本指导原则的通用性,编写中明确本指导原则包含了免疫比浊法、化学发光法、时间分辨法、免疫荧光法等基于抗原抗体反应原理的免疫学方法。由于各种方法可能在国家标准、行业标准的标准性能要求上不一致,如果拟申报试剂已有相应的专用国家/行业标准或相应方法学的通用标准要求发布,则企业标准的要求不得低于上述标准要求。
(三)本指导原则参考了美国食品药品管理局相关要求,但是对心脏CRP部分,考虑到国内已合并至超敏CRP,故本指导原则未保留。同时国内某些公司申请的全程CRP,在临床上没有相应的称谓,也未保留。
四、指导原则编写单位和人员
本指导原则的编写成员由广东省医疗器械注册技术审评人员、行政审批人员、广东省医疗器械质量监督检验中心检验人员、临床专家及相关企业技术人员共同组成。
注:潜在干扰物包括干扰物和交叉反应物。
(一)《体外诊断试剂注册管理办法》(国家食品药品监督管理总局令第5号)
(二)《关于发布体外诊断试剂临床试验技术指导原则的通告》(国家食品药品监督管理总局通告2014年第16号)
(三)《关于发布体外诊断试剂说明书编写指导原则的通告》(国家食品药品监督管理总局通告2014年第17号)
(四)冯仁丰,《临床检验质量管理技术基础》,第二版,上海科学技术文献出版社,2007年4月
(五)Review Criteria for Assessment of C-Reactive Protein (CRP), High Sensitivity C-Reactive Protein (hsCRP) and Cardiac C-Reactive Protein (cCRP) Assays,FDA



C反应蛋白测定试剂盒注册技术审查指导原则
2022年3月18日发布

地址:北京市丰台区西四环南路35号中都科技大厦10层
《互联网药品信息服务资格证书》 编号:(京)一非经营性一2021一0014
备案序号:京ICP备12047146号和京ICP备16030590号 信息产业部备案管理系统网址

扫
一
扫
© 2026北京远博康惠医药信息咨询有限公司 版权所有
北京远博医药CRO
感谢您关注远博医药微信公众号


© 2026北京远博恒康医药科技有限公司 版权所有

商务拓展部(药品&器械)袁经理
电话:010-
邮箱:ybkj045@126.com
人力资源部主任
电话:13146546661
邮箱:ybkj010@126.com
商务总监(药品&器械)薛总
电话:13810708945
邮箱:ybkj027@126.com


◆丰富的临床试验服务经验:
◆熟悉政策法规及审评动态:
◆良好的专家关系:
◆大量临床医院的资源:
◆专业的数据管理:
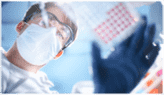
CRO:Contract Research Organization, 出现于上世纪80年代,一种学术性或商业性的科学机构。申办者可委托其执行临床试验中的某些工作和任务,此种委托必须作出书面规定,其目的是通过合同形式向制药企业提供新药临床服务的专业公司。CRO 可以作为制药企业的一种可借用的外部资源,可在短时间内迅速组织起一个具有高度专业化的和具有丰富临床经验的临床队伍,并能降低整个制药企业的管理费用。
 了解更多了解更多
了解更多了解更多







我公司承接国内外厂家或公司的委托,从事药物、医疗器械临床代理服务,以下是我公司服务过的部分项目的名称。














北京远博医药CRO成立于2005年,为医疗企业提供临床试验、项目申报、项目管理和信息咨询等的专业化外包服务(CRO服务),主要为专业化服务内容包括:新药(化药、中药和生物制品)的Ⅰ~Ⅳ临床试验、药代动力学(PK)、生物等效性(BE)、医疗器械的临床试验、上市后再评价、中药保护临床试验、药物经济学等项目的监查及项目管理。
专业化人才优势
绝大多数员工拥有专科以上学历
高标准质量管理体系
必须通过国家药监局高级研修学院的GCP培训并获得证书
完善的培训系统
注重对员工的技术培训,积极参加国家药监总局、药审中心、器械审评中心及各学术团体举办的专业培训及会议;
◆丰富的临床试验服务经验:
◆熟悉政策法规及审评动态:
◆良好的专家关系:
◆大量临床医院的资源:
◆专业的数据管理:
◆优秀而稳定的团队:
◆完善的标准操作流程:
◆独立的质量保障部门:
◆灵活多样的服务方式:

































































































































































































































 预约上门洽谈免费项目咨询
预约上门洽谈免费项目咨询CRO

北京远博医药

临床试验、一致性评价、BE研究和技术服务的专家
专业为医药企业提供一体化的专业技术服务



临床试验优先选择的CRO
18618362640
010-
全国客服热线