




北京远博医药CRO全部业务范围
All of our business scope for you!





总经理致辞
General Manager Address
十多年的创业历程,十多年的辛勤耕耘,造就了今日的北京远博医药。北京远博医药作为中国GCP的早期实践者,以先进的项目管理模式,过硬的质量控制体系、超强的注册审评沟通能力赢得了广大客户的信赖。
作为国内知名的CRO公司,北京远博医药一直致力于药品、医疗器械、医疗产品的临床工作,我们坚持“诚信经营,与客户共赢”的企业宗旨,以诚取信,以信立业。我们将永远履行一个CRO企业应尽的全部义务。希望与广大客户成为永远的朋友,愿我们的事业共同进步!
海以其博大,纳百川而成其浩瀚;山以其厚重,历沧桑而为之雄浑。北京远博医药CRO正以远大的志向,博大的胸怀、诚信务实的品质,敬业创新的态度,科学严谨的作风迎接临床试验外包服务的辉煌未来!
公司简介
About US

北京远博医药是致力于临床试验、科研开发、项目管理和信息咨询的优秀CRO,业务种类包括:新药(化药、中药和生物制品)Ⅰ~Ⅳ期临床试验、生物等效性(BE)研究、药代动力学(PK)、上市后再评价(学术推广)的临床试验、药物经济学评价、循证医学研究、产品指定医院(或领域学术权威专家)的推广型研究、药品上市后增加适应症临床试验、中药品种保护临床试验、医疗器械及诊断试剂的临床试验、处方药转换OTC、进口药物注册申报等。
截止目前,公司已完成和正在进行的临床研究300多项,由我公司负责临床试验并成功获得CFDA批准文号的化药品种共16个、中药7个;我们完成临床获准上市的医疗器械近20个,成功帮助企业获得近60个中药品种的保护证书;同时我们为进入2012版基药目录的6个品种提供了包括上市后再评价、Ⅳ期及药物经济学评价的临床研究服务工作。我们的临床试验专业涉及到呼吸、心脑血管、内分泌、妇科、儿科、泌尿、消化、骨科、耳鼻咽喉、皮肤、血液、口腔、外科、肿瘤、抗生素、麻醉、神经、肝病、抗过敏等诸多领域,已与二百多家医药企业建立了合作关系,在进行临床试验过程中已同400多家药物临床试验机构和三甲医院建立了合作关系。
公司长期以来与国家相关审评、审批部门的合作积累了丰富的政府资源,也与国内多个领域权威医学专家建立了良好的合作关系。公司有一套完善的、符合GCP要求的SOP和质量控制体系,是目前国内承接临床试验项目多、市场推广能力强、中西药并重、政策综合把控好的公司之一。
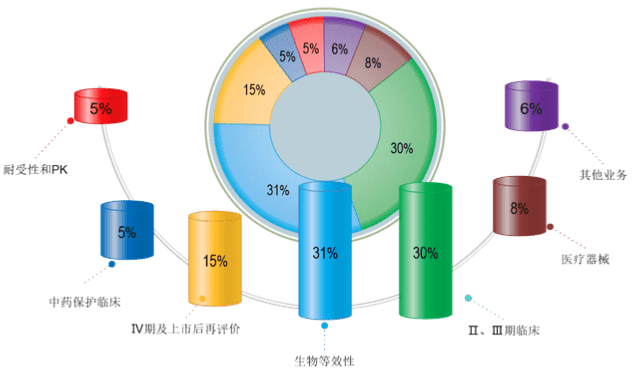
主营业务比例表
Main business chart




300多项临床项目的管理经验
公司建立了一套适合实际操作的SOP,结合独立的数据管理统计及稽查团队设计,既能保证质量又保证项目顺利进行
及时跟踪最新的审评动态及关注政策法规的变化
临床方案须经权威专家审核后方可实施
与400多家临床医院长期合作
主营业务特色及优势
Characters&Advantages

公司有大包模式、小包模式等多种合作模式供客户选择,可为企业合理规避风险同时提高监督效率
管理人员均有5年以上临床经验,并在公司就职3年以上,有丰富的项目管理及专业的项目沟通经验.可规避目前多数CRO由于团队不稳定导致的进度拖延及质量不可控风险
与各审评部门的权威专家有良好的沟通能力
核查通过率100%,未有真实性问题导致的退审



Client Testimonials
客户感言
“我公司一个改剂型的项目不知道如何开展BE研究,北京远博通过与CDE的沟通,明确了审评的要求,对我们公司下一步的决策提供非常重要的信息。”
“我公司通过网上搜索找到了北京远博医药,他们很快就给我们制作了一个BE研究的项目计划书,内容非常全面丰富,为双方的后续合作奠定了一个良好的基础。”
我公司一个多规格的制剂,当初是仿制国内的企业,对如何选择参比制剂确定不了,北京远博医药提供我们全面的国内外文献,并与相关专家进行沟通,解决了这个项目的难点。”
我公司一个高变异性的药物需要进行BE研究,北京远博与国内权威药代专家合作,采用了FDA推荐的针对高变异药物的试验方法,不仅减少了受试者的例数,而且大大节省了费用和时间“
生物等效性试验(BE)
生物等效性试验
生物等效性研究(BE)是一致性评价和化药仿制药申报注册中的重要一环,目前国家药监总局对生物等效性的要求不管是技术要求还是现场核查都基本同美国FDA一致,因此从方案的设计、统计分析的计划、试验的过程运行、统计报告及总结报告的形成都需要非常专业的团队。
Bioequivalence(BE)
生物等效性研究目前还面临着临床医院匮乏的问题,而289个基本药物品种面临着2023年底必须完成的大限。
北京远博医药CRO具有丰富的各种资源,能够为客户提供完整生物等效性研究的CRO服务,包括联系Ⅰ期药物临床试验机构、权威统计分析专家和生物样本测试单位,并对客户全程进行技术指导,按照CFDA最严的核查标准对研究单位的研究过程进行监查及项目管理,尽快协助客户完成生物等效性试验,研究的品种能够尽早完成申报,抢得市场先机。
Why cooperate with us?
服务介绍

开展生物等效性试验
按照国家食药监总局(CFDA)的最新要求
1、新注册分类前的化药6类已经获得临床批件的品种可以制剂开展生物等效性研究;
2、新注册分类后的化药4类品种需要按照备案制的程序进行生物等效性研究;
3、在2022年前批准上市的化药仿制药,需要进行质量和疗效一致性评价,其中口服固体制剂需要按照备案制的程序进行生物等效性研究。

我公司提供整个流程的一站式服务
- 项目的详细调研及联系合作单位
- 起草方案、统计分析计划等
- 项目的启动、监查及管理
- 形成统计分析及总结报告并交接
- 接受药监部门的现场核查
- 协助客户进行项目的注册跟踪




业务优势1:合作单位众多
北京远博医药与国内大量的单位进行过合作,涉及BE研究的有:北京医院、阜外医院、上海市药物代谢中心、上海市药检院、上海中医药大学的统计专家、第四军医大学的统计专家、中国药科大学权威药代专家等等一系列的临床医院和生物样品测试单位,在合作过程中熟悉各家机构的特点及优势,会根据客户项目的特点及要求选择最合适的合作单位进行该项目的生物等效性研究
业务优势 2: 注册沟通能力强
我公司与药审中心(CDE)、中检院等政府审评部门有良好的沟通渠道,可根据国家食药监总局及其下属部门的相关法规、指导原则等要求进行项目的设计及研究,尤其在目前各种政策频出,尤为重要
业务优势 3: 最新的技术标准
近期CFDA频频发布关于临床试验的相关政策、法规要求及技术指导原则,我公司将按照CFDA颁布的最新的技术要求,按照CFDA最严的核查标准要求来进行生物等效性研究的CRO服务,保证项目运行的质量
业务优势 4: 丰富的经验
北京远博医药从事过很多仿制药BE项目的CRO服务,积累了丰富的项目监查管理的经验,公司按照最新的核查标准及技术要求制定了质量管理体系及SOP,并严格要求按照质量管理体系及SOP进行项目的组织、协调、监查及管理等服务,保证项目运行质量
业务优势 5: 技术难点的把握
北京远博医药对生物等效性研究中参比制剂的选择、预BE及正式BE的设计、高变异性药物、长半衰期药物、溶出曲线与BE的关系、招募受试者及受试者的管理等BE过程中难点都有很好的理解及解决办法





Successful Case

我公司服务过生物等效性的相关案例展示
*出于本公司对已合作业务伙伴的信息保密,仅选择性公布部分项目案例

左氧氟沙星片
缬沙坦胶囊
二甲双胍片
阿戈美拉汀片
阿仑膦酸钠片
赖诺普利片
氯雷他定片
孟鲁司特钠颗粒

拉米夫定胶囊
苯磺酸氨氯地平片
吲达帕胺缓释胶囊
瑞格列奈片
布洛芬颗粒
阿托伐他汀钙片


格列美脲片
头孢地尼胶囊

氯吡格雷片
厄贝沙坦氢氯噻嗪片
卡托普利片
阿昔莫司胶囊
阿奇霉素片
坎地沙坦酯片
格列吡嗪片
维格列汀片

我公司生物等效性服务的合作流程
Service Process
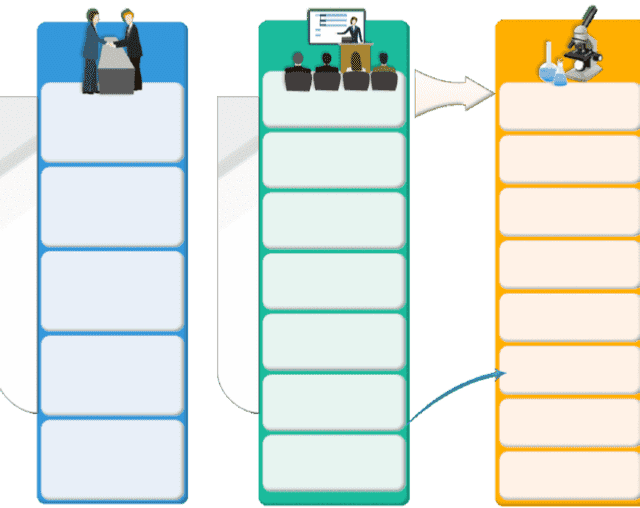
项目洽谈阶段
项目进行阶段
客户接洽
项目调研
制作BE项目计划书
双方项目洽谈
签订合同项目合作
确定GCP基地
方案设计,知情同意书, CRF表制定
申办者提交相关资料
伦理委员会批准
按照CFDA257号文进行备案
申办者提供样品等并启动试验
受试者分组并正式开始试验(药品分发,样品采集,临床监护,不良反应及不良审件的记录与处理)
血样检测单位
生物样品分析方法
根据药物理化性质及文献 资料选择相应的分析方法
方法学确证
方法学质控
样品处理和检测
结果的统计分析,检测
总结报告
合作

项目申报阶段
向客户交接资料
申办者递交资料
药监部门现场核查
项目进行审评
获得批准文号



北京远博医药CRO
© 2026北京远博医药CRO 版权所有




临床试验、一致性评价、项目管理和信息咨询专家
临床试验优先选择的CRO
专业为医药企业提供一体化专业咨询服务








