cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;
附件4
中药新药治疗恶性肿瘤临床研究
技术指导原则
一、概述
恶性肿瘤是严重威胁人类生命的常见病、多发病,尽管现有治疗手段取得了一定疗效,但恶性肿瘤患者仍然缺乏有效的可以治愈的药物。随着近年来肿瘤基础研究的不断进步和对恶性肿瘤疾病认识的不断深入,新的作用机制、作用靶点的抗肿瘤药物不断涌现,呈现出不同于以往传统治疗药物的安全性和有效性特点。治疗恶性肿瘤药物的有效性评价也从以肿瘤客观缓解率(Objective Response Rate,ORR)转变为以延长肿瘤患者的总生存期(Overall Survival,OS)、改善生活质量(Quality of Life,QOL)、减轻身体机能衰退或肿瘤相关症状等,即以恶性肿瘤患者直接的临床获益为有效性评价依据。
中医药治疗肿瘤有二千多年的历史,在古代医籍中,最早提出“癌”的是宋代的《卫济宝书》。古代医家治疗肿瘤的经典方药/方剂也传承应用至今,如小金丹、西黄丸、大黄䗪虫丸、六神丸、片仔癀、桂枝茯苓丸、海藻玉壶丸、当归龙荟丸、梅花点舌丹等,这些传统药方多具有清热解毒、软坚散结的作用,在改善临床症状、抑制肿瘤生长方面显示出了一定疗效。中医认为肿瘤的发生多与毒、虚、瘀等相关,中医治疗肿瘤本着“治病必求其本”的原则辨证施治,始终贯穿着“调整阴阳”“扶正祛邪”“标本兼顾”“病证结合”“内外合治”等中医治疗大法,现阶段治疗恶性肿瘤中医治疗基本原则主要包括扶正培本、活血化瘀、清热解毒、软坚散结、燥湿利水等。
肿瘤中药新药的研发,应根据近年来中药新药治疗恶性肿瘤的临床优势与特点,以及现代医学治疗肿瘤的最新进展,明确在肿瘤治疗中的临床定位、具体适应症,并应具有公认的临床价值。
本指导原则所提出的要求,只是药品监管部门目前较为一致的看法和认识,具有阶段性的特点。除了药品监管法规和技术要求中所规定的内容之外,其他不要求必须强制执行。如果申请人能够有充分的科学证据说明临床试验具备科学性、合理性,也同样获得认可。此外,随着医学科学和医疗实践的发展,疾病诊断、治疗手段等不断的改进,临床试验的要求也会随之更新,因此,本指导原则也会伴同医学科学的进步,在更加科学、合理和方法公认的基础上,及时更新修订。
需要特别说明的是,本指导原则不能代替申请人根据具体药物的特点进行有针对性的、体现药物作用特点的临床试验设计。申请人应根据所研究药物的特点和临床定位,在临床前研究结果基础上,结合学科进展以及临床实际治疗情况,并遵照药物临床试验质量管理规范要求,以科学的精神、严谨的态度,设计与实施临床试验,以客观评价中药新药治疗恶性肿瘤的有效性与安全性。
二、临床定位
现阶段中药新药治疗恶性肿瘤的临床定位通常可分为三类:
第一类:肿瘤治疗用药
以生存期延长和/或生活质量的改善作为主要疗效指标,同时瘤灶缩小或持续稳定等为前提条件。需要注意生活质量需要严格定义,如仅以生活质量改善作为主要疗效指标,临床试验至少需要安慰剂对照。此类定位的中药新药研究一般涵盖如下内容:
1.单独使用中药治疗。具体可参考已发布的《抗肿瘤药物临床试验技术指导原则》。
2.中药联合化疗、放疗、靶向药物等常规治疗增加其临床疗效。具体可参考已发布的《抗肿瘤药物临床试验技术指导原则》。
3.手术、化疗、放疗、靶向药物等常规治疗后的中药巩固治疗或维持治疗。
第二类:肿瘤治疗辅助用药
在不影响原有常规治疗方法(如手术、放疗、化疗等)疗效的前提下,预防和/或减轻肿瘤治疗所致的不良反应的药物。
1.以单一不良反应为治疗目的,例如:放疗后的口干,化疗后的呕吐等。
2.以复合症状群为治疗目的,应选择放化疗等常规治疗相关的主要不良反应。
3.作为预防用药,应预先明确放化疗等常规治疗相关的不良反应发生率或程度,或选择可预期发生不良反应的适应人群。
现阶段不建议以调节免疫功能为主要试验目的。
第三类:改善肿瘤症状用药
以改善肿瘤相关的主要症状为疗效指标,包括癌性疼痛、癌性发热、癌因性疲乏等。
改善肿瘤症状的有效性评价应采用公认的量表及评价标准,并注意体现中医辨证论治的原则,根据药物组成特点,考察中医证候疗效。
三、临床试验要点
(一)在符合临床试验一般原则及要求的基础上,需考虑肿瘤疾病的特殊性及用药特点,采用公认的中、西医诊断标准,病理诊断明确,病种、类型和治疗方法尽量统一。
(二)在伦理允许情况下,应强调随机、盲法的应用,尤其是确证性研究阶段。中药新药在改善肿瘤患者症状、提高生活质量、延长生存期、提高疾病控制率(Disease Control Rate,DCR)等方面的作用具有临床治疗优势与特色,因而在强调以患者生活质量量表、无进展生存期(Progression-Free Survival,PFS)、客观缓解率(ORR)等作为疗效评价指标进行临床试验时,应采用随机盲法,以客观说明中药新药的疗效。
(三)安全性:安全性考察内容除了应符合中药新药临床试验常规安全性观察要求之外,还应重点关注Ⅰ、Ⅱ期临床试验和非临床研究观察到的毒性、蓄积毒性以及少见毒性反应。
如临床定位为肿瘤治疗辅助用药,还需观察常规治疗方法的不良反应,并加以鉴别。
如为合并治疗,应注意药物之间的相互作用。
不良反应的评定采用国际公认通用的抗癌药物毒性分级标准。
(四)中药复方制剂的研究。鉴于恶性肿瘤的疾病特点,中药复方制剂的研究建议应在遵循中医基础理论和临床实践基础上,采用辨病治疗为主,临床前需要提供针对某一类型肿瘤有效的研究证据。
中药复方制剂中医证候的验证需注意“方证对应”,每一种治疗原则有对应的一组证候,如清热解毒药物对应的证候是:发热、肿块增大、局部灼热、疼痛、口渴、便秘等复合症状,因此中药复方制剂需在辨病的基础上明确证候分型以及复合症状范围。在临床症状信息采集和评价方面避免医生单方面主观判断的弊端。建议有来自医生和患者的双重评估。
(五)中药有效成份制剂或有效部位制剂的研究。应依据药理毒理、作用机制等研究结果作为临床试验具体肿瘤类型和临床定位的确定依据,结合现代医学治疗手段的研究进展选择肿瘤的具体适应症、疾病分期、适应人群等。在早期临床试验需进行中医证候探索、剂量探索等研究,为Ⅲ期确证性研究提供依据。
(六)基于目前中医药肿瘤治疗领域的研究进展,《中药新药临床研究指导原则》(2002版,试行)中的肿瘤部分仅供参考。
四、肿瘤治疗用药设计要点
肿瘤治疗用药是指以生存期延长和/或生活质量的改善作为主要疗效指标,同时瘤灶缩小或持续稳定为前提条件。
中药新药肿瘤治疗用药应预先明确是用于治疗某一相同类型肿瘤或者不同肿瘤类型的相同中医证候分型的患者,需要通过科学合理设计和良好质量控制的临床试验而进行探索和确证。
(一)受试者的选择与退出
纳入标准:从伦理学角度考虑,如果单独应用药物,以观察有效性为目的的首次临床试验,可考虑纳入没有经过标准治疗、标准治疗失败或不能耐受的患者,或者经标准治疗后需要巩固或维持治疗的肿瘤患者。所选择患者预计生存期3个月以上,卡氏评分(Karnofsky)arn或体力状况评分标准(ECOG)≤2。
在排除标准中应排除既往抗肿瘤治疗的持续效应,并进行详细的规定,如用药前1个月内曾进行抗肿瘤治疗者,或不符合药物洗脱期规定者。
应制定退出标准,如受试者出现不可耐受的毒性或出现蓄积性毒性导致患者无法继续用药者。
(二)有效性指标及评价要求
应根据临床试验目的选择相应的有效性指标。
临床终点指标:总生存期(OS)和/或生活质量(QOL);
公认的替代指标:无进展生存期(PFS),至疾病进展时间(Time to Progression ,TTP)、无复发生存期 (Relapse Free Survival,RFS)和无病生存期(DiseaseFree Survival ,DFS)。
次要疗效指标:客观缓解率(ORR)、疾病控制率(DCR)等。
鼓励具有中医特色的疗效指标,如中医证候分级量化指标等。
关于生活质量需要严格定义,有效性需经医生评估/患者评估。如仅以生活质量改善作为主要疗效指标,需要瘤体稳定或缩小、生存期获益或与对照组无差异,临床试验设计至少需要安慰剂对照,选用国际公认的生活质量量表, 尤其在确证性研究阶段。鉴于现阶段国际生活质量量表较多,需结合适应症和中药新药具体作用特点,预先进行充分评估,选择恰当的、公认的国际生活质量量表,并需注意对研究者的培训,以保证生活质量量表评价的一致性。
肿瘤相关的检查:应以治疗前后对应的CT或MRI作为影像学检查手段,可酌情监测肿瘤标志物,定期评估,评价指标和方法需建立或遵循严格、客观的质量控制体系。
PFS的检测时点要求:PFS是指从随机化到患者出现肿瘤进展或死亡的时间,可参考已发布的《抗肿瘤药物临床试验技术指导原则》。质量控制要求:在试验方案中应仔细对肿瘤进展标准进行定义。在试验方案和统计分析计划(SAP)中应详细描述评价、测量和分析PFS的方法学。针对数据缺失等现象,试验方案应对每位患者定义何为一个充分的评价随访(即在此次随访中完成了所有约定的肿瘤评价)。由于可以从多个时间、多种来源获得病情进展数据(包含计划外随访的身体检查和各种类型的影像学扫描),因此每次评价随访进行的数据收集有必要在随访前后限定的较短时间内进行。
(三)安全性指标及评价要求
应根据肿瘤药物的特点,如前期非临床安全性评价或早期的临床研究发现的潜在安全性风险,以及处方组成中潜在的安全性风险,设计有针对性的、敏感的安全性检测指标和观测时点。
需充分考虑到肿瘤的疾病特点、合并治疗等临床实际治疗的复杂情况,全面收集安全性数据,对所有不良事件解释要符合医学逻辑,对严重不良事件和重要不良事件等要有详细表述与分析。同时要关注和比较同类药物的安全性问题等。
(四)给药方案
根据临床定位和临床试验目的对肿瘤类型、用药阶段、给药剂量、给药间隔、疗程、合理的剂量调整以及联合放、化疗方案等进行预先的规定。
1.中药新药作为单独治疗用药:一般持续应用到疾病进展或出现不可耐受的毒性,但应制定合理的访视时点,对于晚期肿瘤且已有预期生存时间的,可以预先固定疗程。
2.联合现代常规治疗(手术、放疗、化疗、靶向治疗等),提高治疗疗效的药物疗程原则上需要和常规治疗疗程一致,但可依据不良反应出现的持续时间或程度进行适当调整。
3.手术、化疗、放疗、靶向等现代常规治疗后的中药巩固或维持治疗,疗程需要依据不同病种及不同的治疗阶段而合理设定,一般用药持续到疾病进展或毒性不能耐受。
疗程和访视时间点需依据病种、分期等制定;生存期评估需合理设定,一般每3个月一次。
五、肿瘤治疗辅助用药设计要点
近年来,现代医学治疗肿瘤的方法有了很大的进展,除了传统的手术、放化疗以外,还有生物、免疫疗法、分子靶向以及相应的综合治疗等,得到越来越广泛的重视和应用。这些常规方法在治疗肿瘤的同时,也产生一定的毒性,如出现恶心呕吐、食欲减退、乏力、脱发、皮疹、便秘以及心肝肾脏器损害,骨髓抑制等。
中药新药肿瘤治疗辅助用药的研发,应该和肿瘤学科的发展和进步相适应,并应充分考虑中医临床实际治疗的优势与特点,在不影响放疗、化疗等现代医学治疗方法疗效前提下,减轻常规治疗方法所致的不良反应,如鼻咽部放疗后的口干,化疗时消化道反应、外周神经毒性、皮肤毒性反应、心肝肾功能损伤等,并应考虑病种、放疗、化疗等治疗方案对中药新药有效性、安全性评价的影响。
作为中药新药肿瘤治疗辅助用药,应具有降低手术、放疗、化疗等常规治疗方法和手段导致的不良反应的作用,即中药新药能预防或者改善手术、放疗、化疗等现代常规治疗方法和手段导致的单一症状或复合症状群,但这些症状(群)不能与肿瘤本身发展变化产生的症状(群)相混淆,如肿瘤本身发展变化产生的贫血、腹痛、腹胀、便秘等。
对于以治疗单一症状为试验目的的中药新药:建议选择有代表性的药物或治疗手段所致的单一症状。例如:放疗后的口干、化疗后的呕吐(如顺铂所致)。在某些情况下,如治疗放疗后口干单一症状的药物,可以不仅限于鼻咽癌,还可以包括各种接受相同部位放疗的肿瘤患者。
对于以改善复合症状群为试验目的的中药新药:出现2个或2个以上同时存在且相互关联的症状可以构成复合症状群,如消化道症状群:恶心-呕吐-食欲减退症状群,靶向治疗症状群等。症状群治疗应以中医辨证施治和整体理论为指导,突出中医治疗特色。在观察由于现代常规治疗方法和手段导致的症状群疗效时,尽量选择引起复合症状群严重程度相似的病种、治疗方案和剂量,以避免造成偏倚,同时建议选择有代表性的常规治疗方法和手段。
对于以预防不良反应为试验目的的中药新药:应预先明确原常规治疗方法所致不良反应发生率、严重程度及特点,作为选择预期发生不良反应的适应人群、干预时间、周期等的依据。
中药新药作为肿瘤治疗辅助用药,临床试验主要目的:观察药物预防或减轻常规治疗方法不良反应(包括单一症状、复合症状群、以及脏器功能损伤等)。次要目的:观察药物对常规治疗方法疗效的影响。
(一)有效性指标及评价要求
如治疗单一症状为试验目的:应参照国内外公认的不良反应量表及评价标准观察和评价,也可以采用消失率/复常率评价。
如以治疗复合症状群为试验目的:以复合症状群作为主要疗效指标和疗效评价标准需被公认,如按中医理论指导进行辨证治疗,则中医证候诊断和评价标准需被公认,应依据所选择治疗方案、药物特点、中医证候演变规律设定足够的疗程。
如以预防不良反应为试验目的:应预先明确常规治疗所致不良反应的发生率和程度,尽量选择可预期发生不良反应的适应人群。不良反应发生率需要得到公认,提供预计减轻不良发生率的依据、预期的疗效、干预的时间、疗程等。
(二)给药方案
根据试验目的,一般应与放化疗等治疗周期同步,确定合理的疗程,必要时设计随访。
六、改善肿瘤症状用药设计要点
肿瘤患者因其自身疾病的特点,往往伴随一些常见的临床症状,如癌性疼痛,癌性发热,癌因性疲乏等。与肿瘤治疗用药及肿瘤辅助用药不同,改善肿瘤症状用药是以改善肿瘤本身所致的上述症状作为主要疗效指标。
在符合伦理学的前提下,建议采用安慰剂对照,如为阳性药物对照,阳性对照药物应为已上市的、有充分临床研究证据,且当前临床普遍使用的同类药物中疗效较好的药物。
对于改善肿瘤症状用药,疗效评价应采用国际公认的量表。中医证候诊断和评价标准需被公认。



20151103中药新药治疗恶性肿瘤临床研究技术指导原则
2022年3月18日发布

地址:北京市丰台区西四环南路35号中都科技大厦10层
《互联网药品信息服务资格证书》 编号:(京)一非经营性一2021一0014
备案序号:京ICP备12047146号和京ICP备16030590号 信息产业部备案管理系统网址

扫
一
扫
© 2026北京远博康惠医药信息咨询有限公司 版权所有
北京远博医药CRO
感谢您关注远博医药微信公众号


© 2026北京远博恒康医药科技有限公司 版权所有

商务拓展部(药品&器械)袁经理
电话:010-
邮箱:ybkj045@126.com
人力资源部主任
电话:13146546661
邮箱:ybkj010@126.com
商务总监(药品&器械)薛总
电话:13810708945
邮箱:ybkj027@126.com


◆丰富的临床试验服务经验:
◆熟悉政策法规及审评动态:
◆良好的专家关系:
◆大量临床医院的资源:
◆专业的数据管理:
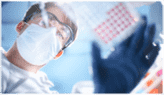
CRO:Contract Research Organization, 出现于上世纪80年代,一种学术性或商业性的科学机构。申办者可委托其执行临床试验中的某些工作和任务,此种委托必须作出书面规定,其目的是通过合同形式向制药企业提供新药临床服务的专业公司。CRO 可以作为制药企业的一种可借用的外部资源,可在短时间内迅速组织起一个具有高度专业化的和具有丰富临床经验的临床队伍,并能降低整个制药企业的管理费用。
 了解更多了解更多
了解更多了解更多







我公司承接国内外厂家或公司的委托,从事药物、医疗器械临床代理服务,以下是我公司服务过的部分项目的名称。














北京远博医药CRO成立于2005年,为医疗企业提供临床试验、项目申报、项目管理和信息咨询等的专业化外包服务(CRO服务),主要为专业化服务内容包括:新药(化药、中药和生物制品)的Ⅰ~Ⅳ临床试验、药代动力学(PK)、生物等效性(BE)、医疗器械的临床试验、上市后再评价、中药保护临床试验、药物经济学等项目的监查及项目管理。
专业化人才优势
绝大多数员工拥有专科以上学历
高标准质量管理体系
必须通过国家药监局高级研修学院的GCP培训并获得证书
完善的培训系统
注重对员工的技术培训,积极参加国家药监总局、药审中心、器械审评中心及各学术团体举办的专业培训及会议;
◆丰富的临床试验服务经验:
◆熟悉政策法规及审评动态:
◆良好的专家关系:
◆大量临床医院的资源:
◆专业的数据管理:
◆优秀而稳定的团队:
◆完善的标准操作流程:
◆独立的质量保障部门:
◆灵活多样的服务方式:

































































































































































































































 预约上门洽谈免费项目咨询
预约上门洽谈免费项目咨询CRO

北京远博医药

临床试验、一致性评价、BE研究和技术服务的专家
专业为医药企业提供一体化的专业技术服务



临床试验优先选择的CRO
18618362640
010-
全国客服热线