cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;cro企业,cro公司,cro,北京cro,北京cro公司,北京cro企业;

地址:北京市丰台区西四环南路35号中都科技大厦10层
《互联网药品信息服务资格证书》 编号:(京)一非经营性一2021一0014
备案序号:京ICP备12047146号和京ICP备16030590号 信息产业部备案管理系统网址

扫
一
扫
© 2026北京远博康惠医药信息咨询有限公司 版权所有
北京远博医药CRO
感谢您关注远博医药微信公众号


© 2026北京远博恒康医药科技有限公司 版权所有

治疗神经病理性疼痛药物临床设计的考虑要点
发布时间2022/4/1 星期五
赵德恒 耿莹 杨焕
神经病理性疼痛(Neuropathic Pain)是指外周或中枢神经系统病变所引起的疼痛。除了患者通常描述的疼痛类型(烧灼痛、放射痛、刺痛、电击样等)外,还可包括感觉缺失、感觉迟钝、触诱发痛和痛觉过敏等症状的组合。疼痛持续或长或短、可呈波动性或周期性,有些是难以预测的。此外,神经病理性疼痛常会伴有情绪变化、睡眠障碍、疲劳等症状,对患者的社会功能造成不利影响。神经病理性疼痛是非特异性的,其发生机制并非某个特定疾病的必然结果。因此,通常是基于病因进行分类,如代谢性或营养性、创伤性、缺血性、神经毒性、免疫介导和压迫性等,而非依据原发疾病。临床试验中获取的有效性数据也是以病因分类为基础的。由于神经病理性疼痛机制复杂,治疗困难,研发治疗神经病理性疼痛的药物一直是一个热点。目前用于治疗的主要药物包括抗抑郁药、抗癫痫药、局麻药、阿片类药和非甾体抗炎药,一些新药处于研发中。本文参考了欧洲药品管理局(European Medicines Agency,EMEA)发布的《神经病理性疼痛治疗药物的临床研究指导原则》,简要介绍了临床研究设计相关的考虑要点,旨在为此类新药的研发提供参考。
1.药理学/药代动力学/药物相互作用研究
采用合适的人体神经病理性疼痛替代模型进行药理学试验,确定药物治疗疼痛的中枢神经系统效应(如镇静、抗抑郁作用)及安全性特征。依据相关指南,结合适应症、疗程、给药方式和途径,以及目标人群的特点,制定合理的研究方案,进行人体药代动力学和药物相互作用研究。
2.剂量探索研究
许多对神经病理性疼痛有治疗作用的药物最早是被用于其他治疗领域的,因而针对原有适应症已经进行过剂量探索试验。然而,在缺乏充分的证据证实其可用于治疗神经病理性疼痛的有效性和安全性时,需要针对新适应症进行剂量探索研究。在对剂量反应曲线进行分析时,需把不良事件考虑在内,在确保用药安全的前提下探索适宜的剂量范围,并使用安慰剂对照。
3.确证性临床试验
3.1.目标人群及入选标准
应招募符合目标适应症诊断的受试者。目前已明确的神经病理性疼痛类型包括带状疱疹后神经痛、痛性糖尿病神经病变、三叉神经痛和中风后疼痛。如果在研究方案中对症状特征给出了明确且充分的定义,其他周围和中枢神经病理性疼痛类型也可作为适应症。
应根据临床病史和检查做出诊断。入选患者应纳入中度至重度疼痛患者(如视觉模拟评分法(Visual Analogue Scale, VAS)≥4分或数字疼痛强度量表(Numerical Rating Scale, NRS)≥4分)。允许入选轻度疼痛患者,但需要考虑到轻度疼痛患者中可能出现的较高的安慰剂效应。由于神经病理性疼痛通常是慢性的,因此符合入选标准的患者的疼痛持续时间应大于3个月。在排除标准中,应考虑以下几项:严重抑郁症,与神经病理性疼痛无关但可干扰疼痛评价的神经或精神疾病,其他可能会妨碍神经病理性疼痛评价的重度疼痛。
数据收集应考虑到疼痛特征和疼痛部位。应使用经过验证的仪器采用标准化的定量测试(如von Frey细丝设备或标准化热设备)对感觉异常进行评价,以揭示针对不同疼痛的不同治疗方式的有效性差异。鼓励对疼痛分布(如病人疼痛图)进行调查,因为疼痛扩展至神经损伤区以外被认为是中枢敏化的诊断线索。在伴有神经病理性疼痛(如卡压综合症、多发性神经病)的疾病中,电生理指标可能会改变,但是它们与疼痛进展(改善或加重)无关。因此,虽然电生理学研究被认为是解释病因的有用工具,但不应将其用作诊断过程的一部分来描述疼痛本身。
3.2.对照的选择
应采用随机、双盲、安慰剂对照的研究设计。如果已有确切疗效的药物获得批准上市用于某个适应症的治疗,那么应采用3臂试验设计(试验药-阳性对照药-安慰剂),以评价新药相对于已有治疗药物在有效性和安全性方面的优劣。
3.3.样本量及分层
研究可能会设计多个固定剂量组,在关键的推荐剂量组应有足够的受试者数量。有充分理由的前提下,安慰剂组患者数量可少于试验药物组。应选择在诊断或症状构成方面具有同质性的患者人群。必要时,可以根据基线疾病病人特征进行分层。试验期间改变治疗的患者,如转为接受新的治疗或其他治疗方法,应作为无反应者来评价。神经病理性疼痛与情绪、躯体及社会功能方面的变化相关,如果研究的目的涉及疼痛以外的其他方面,如睡眠和功能,则应根据具体目的进行研究设计。由于电生理指标和感觉评价与神经病理性疼痛的严重程度无关,因此这些评价不能被用作主要疗效指标,但是这些变量可以用于提供分层标准。
3.4.疗程
观察时间的确定应考虑到神经病理性疼痛的慢性病程特点。观察时间应在达到稳定剂量后继续至少12周,以排除短暂疗效的可能。收集长期安全性数据时,可开展无安慰剂对照的6-12个月开放扩展期研究。与双盲阶段相比,扩展期研究同样需要在严格的质量控制及监查下进行。
3.5.评估时间点
疼痛发作的特点不同,有些是间歇性阵发性的(如三叉神经痛),有些是持续性的,有时二者共存,此外,还有完全诱发的疼痛。评价时间点由研究者依据疼痛发作特点来确定,通常认为在同一天的早晨和晚上各进行一次评估是合理的。可以采用患者日记卡自评的方式进行评估。按照试验方案设计日记卡,确保能够采集到所需要的信息。患者使用日记卡进行疼痛评估时可能存在一些问题,如依据回忆来评估疼痛或不能按时完成日记卡等,这些问题需要被关注并在评估进行前对自评方法给予指导,以避免评价的偏倚。
3.6.伴随治疗
对于疼痛的临床研究,应特别注意非药物治疗及合并用药对试验的影响。在试验期间,应尽量避免使用任何可改变疼痛感知的非药物治疗方法(如物理方法、手术和心理治疗),如果不可避免,应在试验期间维持该治疗的稳定。合并使用影响疾病进展的药物(如降糖药、抗病毒药物)有时不可避免,应在试验期间保持这些药物的剂量稳定。对试验之前的合并用药应允许有适当的洗脱期,以确保其在进入研究前已被消除。如果允许使用急救药物,应对使用情况进行记录,并分析其对药物疗效的影响。
3.7.统计分析和结果报告
应遵循现有指南(ICH E9:临床试验的统计学原理)进行统计分析及结果报告。情绪变化、睡眠障碍或疲劳以及一些与药物有关的不良事件(如头晕或嗜睡)可能会改变对疼痛的感知,进而影响对药物有效性的评价,这些因素需在有效性分析时加以考虑。在方案中应对可以使用的急救药物及使用方法给出规定,应分析急救药物对观察结果的影响,原则上不提倡使用超过一种以上的急救药物。此外,在评价时还应考虑到患者或医生处于非盲态时可能影响对药物疗效的判断。可以在疗效不充分的已有治疗基础上开展附加治疗的研究,但是研究的结果仅限于提示附加治疗的有效性。需评价对照组和试验组人群的同质性,还应评价试验人群既往使用治疗神经病理性疼痛的药物的暴露和反应,通常需要对既往有反应者和无反应者进行亚组分析,分析结果会影响到对试验结果的解读。
3.8.有效性评价方法
应依据疼痛类型和特征选择合适的量表进行评估。一维疼痛量表,如视觉模拟评分法(Visual Analogue Scale, VAS)或数字疼痛强度量表(Numerical Rating Scale, NRS),已被广泛用于神经病理性疼痛严重程度的评价,并已在临床研究中得到充分的验证。另有一些多维度量表也可用于评价神经病理性疼痛在各维度的特征,如神经病理性疼痛量表(Neuropathic pain scale,NPS)、神经病理性疼痛症状量表(Neuropathic Pain Symptom Inventory, NPSI)、简明McGill疼痛问卷(Short-form of McGill Pain Questionnaire, SF-MPQ),但这些量表比较新尚未被广泛使用,故仍待在试验中被充分验证。用于评价感觉迟钝、触诱发痛或痛觉过敏的评估工具也可作为支持性证据用于对疗效进行评价。
主要疗效终点 主要疗效终点包括使用问卷对疼痛程度进行的评价,可以是一维量表,如VAS或NRS,或经验证可用于神经病理性疼痛的多维评价问卷。建议使用应答率来评估疼痛的改善。应答率是指,与基线相比,疼痛量表减分率达到30-50%的患者比例。建议将试验组间疼痛应答率的比值作为主要疗效终点。对疼痛应答的不同界值应进行灵敏度分析。疼痛应答也可以被定义为减分,例如疼痛程度相比于基线(0-10级)减少了2分,确定界值同样需要进行灵敏度分析。
次要疗效终点次要疗效终点包括对感觉迟钝、触诱发痛或痛觉过敏、变化刺激激发的疼痛、情绪和睡眠的评价,社会功能量表以及生活质量量表评估等。根据次要研究目的,确定次要终点和对应使用的评估工具及其优先级。需要对使用到的评价工具进行验证,对刺激诱发的疼痛、触诱发痛或痛觉过敏的测试应使用已校准的设备进行标准化定量的感觉测试。电生理变量不宜作为研究终点。
3.9.安全性评价方法
应根据ICH指南要求对与试验药物相关的不良事件(AE)进行监测。应采用系统的有计划的方法,根据药物作用机制,对潜在AE进行评价。应按躯体系统详细记录AE。识别AE风险高危人群。对某些已用于治疗神经病理性疼痛的药物,应评估与其相关的不良事件,如阿片类药物可能出现的恶心、便秘、嗜睡、头晕;三环类抗抑郁药的镇静和抗胆碱能作用;抗癫痫药可能出现的皮疹、镇静、头晕、恶心等。对于引发神经病理性疼痛的原发疾病,应研究试验药物对其潜在的不利影响(如糖尿病)。应对用于慢性神经病理性疼痛的药物进行至少12个月的长期安全性研究。停药后的撤药反应和反弹效应也应进行评价。
3.10.在特殊人群中的研究
儿童有关儿童与神经病理性疼痛的信息非常有限。在成人研究中较常见的神经病理性疼痛模型,如带状疱疹后、糖尿病多发性神经病变和中风后疼痛很少见于儿童。儿童和青少年中发生的神经病理性疼痛病因多样,较常见的是创伤性神经病理性疼痛、幻肢痛、分娩性臂丛神经损伤和抗肿瘤治疗后疼痛。鼓励采用同时见于成人和儿童的神经病理性疼痛模型(如幻肢痛)进行某种药物的疗效及安全性研究,这样有利于了解如何将有效性数据从成人外推至儿童,或从一种疾病模型外推到另一种疾病模型。研发长期使用的药物需要获得长期安全性数据,以评价药物治疗对儿童生长发育、内分泌水平和认知功能的影响。
老年 大部分神经病理性疼痛研究在相对高龄的患者中进行,因此,通常获得的药代动力学和临床试验数据足以支持对老年人群进行单独的数据分析。由于与某些药物相关的不良事件在老年患者中可能更加频繁和严重(如阿片类、三环类抗抑郁药),因此需要特别引起关注。
4.小结
对神经病理性疼痛发病机制的认识日渐清晰,研发更加安全有效的治疗药物成为临床迫切需求。本文介绍了神经病理性疼痛治疗药物临床研究设计的考虑要点,旨在强调研究设计在药物有效性及安全性评价中的重要性,供参考。以上观点为针对研究设计时的重点内容的一般考虑,仅代表我们当前的认识,欢迎业界和研究者在制定方案过程中,及时与我们沟通和讨论,并提出意见和建议。
参考文献:
[1] Merskey H, Bogdku N. Classification of Chronicpain. Descriptions of Chronic Pain Syndromes and Definitions of Pain Terms, ed 2. Seattle, IASP press,1994, 394.
[2] 舒海华,安坷,李桥波,黄文起.神经病理性疼痛的药物治疗. 实用疼痛学杂志. 2011, 7(2):127-133.
[3] EMA, Committee for Medicinal Products for Human Use. Guideline on clinical medicinal products intended for the treatment of neuropathic pain. http://www.emea.europa.eu.2013-04-23
[4] ICH Harmonised Tripartite Guideline, Statistical principles for clinical trials. http://www.ich.org/pdflCH/e9.pdf,1998-12-09
[5] Huskisson EC. Measurement of pain. Lancet. 1974, 2:1127-1131



商务拓展部(药品&器械)袁经理
电话:010-83659936 18618362640
邮箱:ybkj045@126.com
人力资源部主任
电话:13146546661
邮箱:ybkj010@126.com
商务总监(药品&器械)薛总
电话:13810708945
邮箱:ybkj027@126.com


◆丰富的临床试验服务经验:
◆熟悉政策法规及审评动态:
◆良好的专家关系:
◆大量临床医院的资源:
◆专业的数据管理:
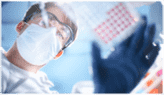
CRO:Contract Research Organization, 出现于上世纪80年代,一种学术性或商业性的科学机构。申办者可委托其执行临床试验中的某些工作和任务,此种委托必须作出书面规定,其目的是通过合同形式向制药企业提供新药临床服务的专业公司。CRO 可以作为制药企业的一种可借用的外部资源,可在短时间内迅速组织起一个具有高度专业化的和具有丰富临床经验的临床队伍,并能降低整个制药企业的管理费用。
 了解更多
了解更多
了解更多
了解更多








我公司承接国内外厂家或公司的委托,从事药物、医疗器械临床代理服务,以下是我公司服务过的部分项目的名称。









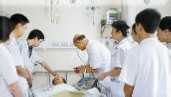





北京远博医药CRO成立于2005年,为医疗企业提供临床试验、项目申报、项目管理和信息咨询等的专业化外包服务(CRO服务),主要为专业化服务内容包括:新药(化药、中药和生物制品)的Ⅰ~Ⅳ临床试验、药代动力学(PK)、生物等效性(BE)、医疗器械的临床试验、上市后再评价、中药保护临床试验、药物经济学等项目的监查及项目管理。
专业化人才优势
绝大多数员工拥有专科以上学历
高标准质量管理体系
必须通过国家药监局高级研修学院的GCP培训并获得证书
完善的培训系统
注重对员工的技术培训,积极参加国家药监总局、药审中心、器械审评中心及各学术团体举办的专业培训及会议;
◆丰富的临床试验服务经验:
◆熟悉政策法规及审评动态:
◆良好的专家关系:
◆大量临床医院的资源:
◆专业的数据管理:
◆优秀而稳定的团队:
◆完善的标准操作流程:
◆独立的质量保障部门:
◆灵活多样的服务方式:

































































































































































































































 预约上门洽谈
免费项目咨询
预约上门洽谈
免费项目咨询CRO

北京远博医药

临床试验、一致性评价、BE研究和技术服务的专家
专业为医药企业提供一体化的专业技术服务



临床试验优先选择的CRO
18618362640
010-83659936
全国客服热线